المناعة في غرس الأنسجة والأعضاء-مقدمة-
المناعة في غرس الأنسجة والأعضاءبداء اهتمام الإنسان بتعويض نسيج أو عضو مريض أو مبتور بأخر سليم مند مئات السنين ، وربما يعود تاريخها إلى عهد ما قبل التاريخ. في البداية كان التركيز منصب علي أجراء الترقيع في الأنسجة الذاتية، كإعادة شفة مقطوعة أو ادن مقطوفة أو مقطوعة أو انف مقطوع.
في عام 1870 إفرنجي قام رفردين (Revrdin) بعملية ترقيع لنسيج جلدي علي شكل بقع صغيرة خصوصا في حالات الجروح الكبيرة لمساعدتها علي الالتئام ، وبعد رفردين جرت محاولات أخرى باستعمال قطع اكبر من نسيج جلد من أشخاص آخرين وإعطائها إلى المصابين وكان في الغالبية العظمي هذة الأنسجة يكون مصيرها الرفض ولم يكن يعرف سبب رفضها في ذلك الوقت وقد ساد اعتقاد بأن سبب الرفض هو الفرق الوراثي بين النسيج المرقع وأنسجة العائل وكان ذلك صحيح إلى حد ما ولكن لم يعرف دور المناعة في هذا الرفض ألا في الأربعينيات من هذا القرن بواسطة ميداور (Medawar).
أول عملية نقل ناجحة كانت لكلية بين تؤمين متشابهين ولكن نقل كلية بين أفراد غير متشابهين لم يكتب لها النجاح ألا بعد استعمال المواد المثبطة للمناعة. وهكذا تبين أن سبب الرفض يعود إلى وجود مستضدات التوافق النسيجي الموجودة علي سطح الخلايا والتي تعكس الاختلاف في الأصل الجيني بين المتبرع والمستقبل لطعم ولذا فأن النسيج المنقول يدمر ويعتمد قتل الطعم (النسيج الغروس) علي تميز الليمفاويات التائية لوجود مستضدات غريبة ودخيلة علي سطح الخلايا ومن تم قتلها ويتم ذلك بدرجة كبيرة من خلال استجابة نوعين من الليمفاويات التائية الأولى الخلايا التائية المساعدة والنوع الثاني الخلايا التائية السامة (القاتلة) للخلايا. ولتحاش رفض الطعم (الرقعة) المخالف يتم فحص الانسجام (التوافق) بين مستضدات فصائل الدم ومستضدات مركب التوافق النسيجي لكل من المستقبل والمتبرع فإذا كانت النتائج توحي بالانسجام ، تتم عملية نقل النسيج. ويمكن تثبيط رفض الطعم المغاير (الغير متطابق) بواسطة استعمال أدوية مثبطة للمناعة ولكن هذا قد يعرض المستقبل إلى أخطار الإصابات المرضية بالجراثيم وخصوصاً الانتهازية منها والسرطانات أحيانا إلى مرض مهاجمة المستقبل من خلال النسيج المنقول.
تصنف الغرس أو الرقع إلى أربعة أنواع وذلك اعتمادا علي العلاقة الجينية بين المعطي والمستقبل :-
أ- الرقعة الذاتية Autograft؛ وهي الرقعة التي تؤخذ من منطقة إلى منطقة أخرى في جسم ذات الشخص. مثل نقل قطعة من جلد الفخذ إلى اليد أو الوجهة لترقيع منطقة محروقة.
ب – الرقعة المشابه (او المتماثلة) Isograft، وهي الرقعة المنقولة من شخص إلى آخر متشابه معه من الناحية الجينية مثل التوائم المتطابقة.
جـ – الرقعة النمطية Allograft، مثل نقل رقعة بين كائنين غير متطابقين من ناحية الجينات ولكنهما ينتميان لنفس النوع (مثل بين شخصين لا توجد علاقة جينية بينهما) وفيما عدا نقل الأنسجة والأعضاء بين التوائم المتطابقين فأن كل حالات نقل الأعضاء والأنسجة بين البشر هي من هذا النوع.
د – الرقعة المغايرة (أو الغريبة) Xenograft، وهو طعم بين نوعين مختلفين من المخلوقات الحية، كنقل عضو من حيوان إلى إنسان وغالبا لا يستعمل هذا النوع لأنة محكوم علية بالفشل التام ألا في الحالات النادرة جدا.
أنماط الاستجابة المناعية TYPES OF Immune Response
أنماط الاستجابة المناعية TYPES OF Immune Response*الاستجابة المناعية الأولية The primary response :
يلي دخول مستضد غريب للجسم (لأول مرة) فترة من التلكؤ (lag period) أو الكمون (latent period) تمتد لعدة أيام قبل أن تكشف الأجسام المضادة في المصل
فترة الكمون latent period أو التلكؤ هذه (تسمى أحيانا فترة الحث induction period) تختلف، فهي قد تستغرق فترة من عدة ساعات إلى عدة أيام اعتمادا علي نوع المستضد وكميتة وطريقة دخوله للجسم، بالإضافة إلى نوع العائل وصحته وحساسية الاختبار المستخدم في الكشف عن الجسم المضاد، ففي العادة يظهر الجسم المضاد (أي يمكن الكشف عن وجود الجسم المضاد في المصل بالطرق المخبرية) خلال فترة من 5 إلى 10 أيام من وقت دخول المستضد للجسم، مع ملاحظة بأن فترة التلكؤ والكمون هذه لا تمثل الفترة اللازمة لبداية إنتاج الأجسام المضادة، ففي الواقع تبدأ الخلايا المنتجة للأجسام المضادة في إنتاج الأجسام المضادة خلال 20 دقيقة من وقت دخول المستضد للجسم وتعرف الخلايا المنتجة للأجسام المضادة علي المستضد، ألا أن الخلايا المنخرطة في إنتاج الأجسام المضادة في البداية تكون قليلة وبالتالي تكون كمية الأجسام المضادة قليلة ولهذا قد تمر عدة أيام قبل أن يكون بالإمكان الكشف عن وجودها في المصل وعامل آخر قد يساهم في عدم الكشف عن وجود الأجسام المضادة في المصل هو ربما أن الأجسام المضادة المنتجة في البداية تجد بقايا المستضد في الدورة الدموية وبالتالي ترتبط بها مكونة معقد مناعي، مما يجعل الكشف عن الأجسام المضادة في هذه الحالة صعب بالاختبارات المصلية المعتادة وبالتالي لا يمكن الكشف عن الأجسام المضاد ألا بعد عدة أيام من دخول المستضد للجسم عندما تكون هناك كمية كبيرة من جزيئات الأجسام المضادة الحرة في المصل، كما أنة عندما تكون كمية المستضدات التي دخلت إلى الجسم كبيرة فهذا أيضا يساهم في إطالة فترة التلكؤ.
– في نهاية مرحلة الكمون تكون استجابة الأجسام المضادة مرئية، كما أن عيار الجسم المضاد يزداد تدريجيا في فترة بعض أيام إلى بعض أسابيع حتى يصل العيار إلى مرحلة استقرار نسبي، تم يبدأ في الهبوط التدريجي إلى أن يختفي أو يثبت عند مستوي معين من التركيز في المصل . تكون الاستجابة المناعية الأولية في صورة أجسام مضاد من نوع IgM الذي بعدة فترة وبشكل تدريجي تحل محلها أجسام مضادة من نوع IgG الذي يبقي هو السائد.
LAG PERIOD is the time between the exposure of the host to an antigen and the appearance of detectable immune response.
*الاستجابة الثانوية The secondary response :
بعد التعرض للمرة الثانية لنفس المستضد الغريب فأن الاستجابة المناعية ضده من قبل العائل تختلف كليا عن الاستجابة الأولية، حيت تكون فورية وقوية والتي تتمثل في سرعة ظهور الخلايا الكفوءة مناعياً (خلايا الذاكرة) والتي تنتج عنها زيادة في كمية الأجسام المضادة المنتجة (أي زيادة كبيرة في عيار الجسم المضاد). – إذا كانت الأجسام المضادة لازالت موجودة في المصل عند حقن الجرعة الثانية من المستضد، فأن الكمية تقل أو تختفي بسرعة بسبب سرعة التفاعل بين الأجسام المضادة الموجودة سابقاً في المصل والمستضد المحقون حديثاً للمرة الثانية مشكلاً معقد مناعي بين المستضد والجسم المضاد (وهذه المرحلة تسمي مرحلة الطور السالب Negative phase). الاستجابة الثانوية تكون عادتاً في شكل أجسام مضادة من نوع IgG مع أنة قد يحدث إنتاج كميات قليلة من الأجسام المضادة من نوع IgM.
– تعتبر كمية الجرعة المحقونة من المستضد مهمة جداً، فإذا كانت الكمية قليلة لا تحدت زيادة في الاستجابة المناعية لأن الأجسام المضاد المنتجة سابقا قد تكون كافية لإزالة المستضد وبالتالي لا يتوفر محفز للخلايا المنتجة للأجسام المضادة، أما إذا كانت كمية الجرعة كافية لأحداث استجابة مناعية فستحدث استجابة مناعية ثانوية أو ما يعرف باستجابة الذاكرة أو الداعمة ((The memory, anamnestic or booster response.
الاستجابة المناعية الثانوية تكون ناتجة عن الذاكرة المناعية (immunologic memory)، التي يعتقد بأنها تحمل بواسطة الليمفاويات الصغيرة.
تختلف الاستجابة المناعية الأولية عن الثانوية في آلاتي-
1- وقت التلكؤ في الاستجابة الثانوية اقل بكثير من وقت التلكؤ في الاستجابة الأولية.
2- تمتاز الاستجابة المناعية الثانوية بسرعة إنتاج الأجسام المضادة وبمستويات عالية وتدوم لفترة أطول.
3- الجرعة اللازمة لأحداث الاستجابة الثانوية اقل بكثير من الجرعة اللازمة لأحداث الاستجابة الأولية.
5- تكون الأجسام المضادة المنتجة في الاستجابة الثانوية غالبا من نوع IgG.
تعتمد قوة الاستجابة المناعية الثانوية علي الفترة بين الجرع المعطاة من المستضد ، بحيث يجب أن لا تكون الفترة قصيرة جداً ولا بطويلة جداً وفي الحالتين تحدت قلة في الاستجابة المناعية. ويعود السبب في ذلك إلى أن المستضد يزال كليا في الحالة الأولى وفي الثانية قد يحصل بسبب هرم الخلايا المتخصصة بالمناعة (أي خلايا الذاكرة) ، مع ملاحظة بأن هذا لا ينطبق على كل الحالات فقد تستمر ظاهرة الذاكرة المناعية لعدة سنين وبذلك تبقي الاستجابة المناعية ضد ذلك المستضد الغريب لفترة طويلة ، ربما لطول فترة الحياة كما يحصل في بعض الإصابات الفيروسية والجرثومية وبالتالي لا يوجد وقت محدد لأحداث أو استثارة الاستجابة الثانوية.
هناك عدة عوامل تحدد قدرة العائل على تكوين استجابة مناعية وتحديد شدة أصابته بالمرض ، من هذه العوامل ما هو خاص بالعائل، مثل الحالة الصحية العامة للعائل وجنسه وعمر حيث أن الإصابة غالبا ما تكون اشد في طرفي العمر (أي في الطفولة والشيخوخة) كما أنها تعتمد أيام علي قدرة وقوة الجهاز المناعي للعائل وأن كان قد تعرض في السابق لذات المرض أو لا ، الليمفاويات العوامل الخاصة بمسبب المرض (المستضد) والتي يكون لها تأثير على شدة المرض فمنها قدرة مسبب المرض على اختراق الحواجز الطبيعية للعائل كالجلد والأغشية المخاطية ..الخ، ومقدرة مسبب المرض على التصدي لدفاعات العائل الطبيعية والمكتسبة مثل وجود محفظة أو إفراز مواد واقية أو القدرة على التملص من الجهاز المناعي ، كما أن لطريقة دخول ونوع وكمية جرعة مسبب المرض دور في تحديد قدرة دفاعات العائل على التصدي له.
أن هذا النوع من الاستجابة المناعية تعتبر استجابة مناعية خلطيه لأنها تعتمد فالتخلص من الجسم الغريب على تكوين أجسام مضادة نوعية ضد الجسم (المستضد) الغريب.
كيفية حدوث الاستجابة المناعية الخلوية –
إذا تم جراحياً إزالة قطعة من نسيج حي (مثل الجلد) لحيوان ما (كلب مثلاً) وتم غرسها في حيوان آخر من نفس النوع (كلب آخر) ولكن لا يوجد بينهما توافق ، فأن الرقعة المغروسة تبقي حية لعدة أيام (حوالي 10 أنة) ومبدئياً تبدو خلالها هذه الرقعة سليمة وتتكون لها أوعية دموية تربطها بالعائل. ولكن بعد أسبوع واحد الأوعية الدموية المتكونة تبدأ في الانحلال (degenerate) ،مما يؤدي إلي توقف تزويد الرقعة المغروسة بالدم مؤدياً إلي موتها ورفضها من قبل العائل. عملية الرفض تلك تكون بطيئة وتسمى First-set reaction. ولا يحدث الرفض بسبب وجود صعوبات جراحية في عملية غرس الرقعة وإنما تشير إلي وجود آلية في جسم الحيوان المستلم يتم بها تميز آدني اختلاف في الخلايا الغريبة عن الخلايا الذاتية للعائل (المستلم) ، مما يؤدي إلي التخلص من الرقع الغريبة بسرعة لا يتوفر الآلية تكمن في الجهاز المناعي للمستلم ، وحتى الخلايا الذاتية التي أصبحت غير طبيعية ولو بشكل بسيط من الناحية التركيبية ربما يميزها الجهاز المناعي على أنها غريبة ويقوم بإزالتها. أن الاستجابة المناعية ضد الخلايا الغريبة من خلال رفض الطعم المغروس تؤكد وجود جهاز إشراف (surveillance) في جسم العائل يقوم بتميز وإزالة الخلايا الغريبة أو الذاتية الغير طبيعية. وإذا ما تم اخذ رقعة أخرى من ذات الحيوان المعطى الأول ونقلت إلي الحيوان المستلم الأول ، فأن الرقعة الثانية لن تبقى لأكثر من يوم أو يومين تم ترفض من قبل المستلم . عملية الرفض السريعة هذه تسمى Second-set reaction ، وهكذا نجد أن عملية الرفض الأولى نسبياً تكون ضعيفة وبطيئة وهى تكون مماثلة للاستجابة المناعية الاولية للأجسام المضادة (الاستجابة الخلطية) ، بينما الاستجابة ضد الرقعة الثانية تحرض استجابة رفض سريعة جداً وقوية مماثلة للاستجابة الثانوية للأجسام المضادة. أن عملية رفض الطعم أو الرقعة مثل استجابة الأجسام المضادة تكون نوعية وتعتمد على الأولية حيث أما Second-set reaction يحدث فقط إذا كانت الرقعة الثانية منقولة من ذات المتبرع الأول الذي نقلت منه رقعة أدت إلي حدوث الـfirst-set reaction كما أما الأولية المتكون عن الرقعة الأول تؤدي إلي تذكر أحداث التعامل مع الرقعة الثانية من قبل الجهاز المناعي للعائل حتى لو تم إعادة غرس رقعة من المعطى الأول الذي قام جسم العائل برفض رقعته الأولى بعد عدة اشهر أو حتى عدة سنوات من بعد الرفض الأول وأيضا يكون الرفض قوي وسريع للرقعة الثانية. مثل هذا النوع من الاستجابة المناعية هي استجابة مناعية خلوية أو ما يعرف أحيانا بالمناعة المتوسطة بالخلايا التي تقوم بها الخلايا التائية. مع ملاحظة بأن الاستجابة ضد الرقع لا تكون استجابة خلوية فقط ولكن تتكون أيضا استجابة مناعية خلطيه (أجسام مضادة) تلعب دور مهم في عملية الرفض والتخلص من الرقع الغريبة عن العائل.
أعداد المستضد Antigen Processing-
في الواقع أن الآلية التي أشير أليها أعلاه في استجابة جسم العائل المناعية ضد المستضدات الغريبة لا تتم بهده البساطة ، وإنما يسبق ذلك أعداد وتقديم للمستضد لتتعرف عليه الخلايا المحدثة للاستجابة المناعية وكذلك لو أن كل المستضدات الغريبة تتم بلعمتها وتحطيمها كليا بواسطة الخلايا الأكولة فليس هناك حاجة لحث المناعة وأحداث استجابة مناعية ولذلك على الأقل جزاء بسيط من المستضد يبقى لاستثارة الخلايا الحساسة للمستضدات الغريبة لأحداث استجابة مناعية لها . البلعميات الكبيرة تعتبر من أهم الخلايا التي لها القدرة على أعداد المستضد (antigen processing) لغرض أحداث استجابة مناعية فاعلة . أن أعداد المستضد يتطلب تقديمه بصورة مناسبة لعدد من الخلايا الحساسة للمستضدات مثل الخلايا التائية المساعدة إذا كان المستضد خارجي (exogenous antigen) ، أو للخلايا التائية السامة إذا كان المستضد داخلي (endogenous antigen) . يتم أعداد المستضد الخارجي على ثلاثة مراحل ، في المرحلة الأولى تقوم البلعميات ببلعمت المستضد الغريب مما يؤدي إلي تحطمه إلي جزيئات ببتيدية قصيرة (تتكون من حوالي 10 إلي 20 حامض أميني) ، والمرحلة الثانية يتم فيها ارتباط الجزيئات الببتيدية القصيرة للمستضد مع الصنف الثاني من مركبات التوافق النسيجي الأكبر (MHC class-II) ، وأخيرا تحمل تلك الجزيئات الببتيدية المرتبطة مع الـMHC class-II إلي سطح الخلية مما يؤدي إلي التعرف علية بواسطة الخلايا التائية المساعدة (T-helper cell) والتي بدورها تقوم بتحفيز (تنشيط) الخلايا الليمفاوية البائية الحاملة لمستقبل المستضد على التكاثر (عمل نسيله) وإفراز أجسام مضادة نوعية لذلك المستضد. الليمفاويات إذا كان المستضد داخلي مثل البروتينات التي تكونها الفيروسات داخل الخلية التي تصيبها ففي هذه الحالة الجزيئات الببتيدية للمستضد ترتبط مع الصنف الأول لمركبات التوافق النسيجي الأكبر (MHC class-I) ، ثم يحمل إلي سطح الخلية مما يؤدي إلي التعرف علية من قبل الخلايا التائية السامة والتي بدورها تقوم بقتل وتحطيم والتخلص من الخلية المصابة بالفيروس بشكل مباشر.
الاستجابة المناعية Immune Response
الاستجابة المناعية Immune Responseعند تعرض الجسم للغزو من أجسام غريبة (مستضدات غريبة) فان الجاهز المناعي للجسم يقوم بدورة لتخلص من الجسم الغريب بواسطة سلسلة من التفاعلات المناعية والتي تعرف بالاستجابة المناعية.
الجهاز المناعي لكي يقوم بعملة بصورة سليمة يحتاج إلي أربع مكونات أساسية هي :-
ا- طريقة لحجز ومعالجة (أو التعامل مع) المستضد .
i- A method of trapping and processing antigen
ب- آلية نوعية لتعامل مع أو التفاعل بشكل نوعي مع المستضد أو بعبارة أخرى خلايا حساسة للمستضد.
ii- A mechanism for reacting specifically to antigen or, in other words, antigen-sensitive cells.
جـ- خلايا لإنتاج الأجسام المضادة أو الاشتراك في المناعة الخلوية .
iii- Cells to produce antibodies or to participate in the cell-mediated immune response.
د- خلايا لتذكر كل المعلومات (الأحداث) عن المستضد والتفاعل معه بشكل نوعي في حالة ما كرر مهاجمة الجسم مستقبلاً .
vi- Cells to retain the memory of all event and to react specifically to the antigen in future encounters.
تحدث تفاعلات الاستجابة المناعية المكتسبة من خلال آليتين رأسيتين هما:
1- المناعة الخلطية Humoral immunity: وهي المناعة المتكونة بواسطة الأجسام المضادة، أي هي الحالة المناعية الناشئة عن إنتاج الأجسام المضادة (الجلوبيولينات المناعية Immunoglobulins) التي تقوم بعملها في غياب الخلايا المناعية التي أنتجتها. وهذه الأجسام المضادة أما أنها تكونت نتيجة التعرض لمستضد حث الخلايا الليمفاوية (خلايا البلازما) علي تكوينها بشكل طبيعي، أو أنها تتواجد بشكل اصطناعي عن طريق إعطاء (حقن) مصل يحتوي علي أجسام مضادة، أو انتقال الأجسام المضادة من ألام إلي طفلها عبر المشيمة (IgG) أثناء الحمل أو عبر الرضاعة (IgA) ، الحالة الأولى ينتج عنها تكون مناعة مكتسبة فعالة طبيعية والحالة الثانية ينتج عنها تكون مناعة مكتسبة غير فعالة (منفعلة) اصطناعية ولذا من الممكن نقل هذه المناعة من شخص لأخر بواسطة نقل الدم (مصل الدم).
2- المناعة الخلوية Cell-mediated immunity:- تنشاء الاستجابة المناعية الخلوية عن الخلايا الليمفاوية التائية والتي تتمكن من إفراز اللمفوكينات (Lymphokines) بعد تعرضها للمستضد والذي يؤدي إلى سرعة تحرك وتنشيط الخلايا البلعمية الكبيرة (البلعميات الكبيرة) لتقوم بعملية مهاجمة الأجسام الغريبة وتقديمها لليمفاويات التائية.
عادتا ينتج عن لاستثارة المناعية الخلوية نوعين من الخلايا هي الخلايا الليمفاوية التائية (الخلايا التائية السامة للخلايا) وحيدة النسلية (monoclonal) والتي تهاجم المستضد (الجسم الغريب) والأخرى خلايا الذاكرة المسئولة عن الاستجابة المناعية الخلوية الثانوية في حالة تعرض الجسم للمستضد الغريب مرة أخرى.
تتولى المناعة الخلوية الدفاع ضد مسببات الأمراض وبصورة خاص التي تتخذ من الخلايا(Intercellular) مكان لها وضد الطفيليات والنسيج الغير متوافق المنقول للعائل وتدمير الخلايا السرطانية ، كما أنها تدخل في أحداث تفاعلات فرط الحساسية.
يشارك في المناعة الخلوية بالإضافة إلى الخلايا التائية والبلعميات الكبيرة ، خلايا أخرى مثل الخلايا القاتلة والخلايا القاتلة الطبيعية والخلايا الملتهمة (الأكولة) وحيدة النواة.
إزالة المستضد (الغريب) Elimination of antigen:
في حالة حقن مستضد غريب في الوريد فأن أزالته ذلك المستضد تتم عبر ثلاثة مراحل هي :
المرحلة الأولى The first phase :
هذه المرحلة تستغرق من 10 إلى 20 دقيقة إذا كان المستضد المستعمل دقائقي (غير ذائب) ، وهذا الوقت اللازم لتوازن المستضد في الأنسجة والسوائل ، حيث أنه تقريبا 90% من المستضدات تتم أزالته خلال دورتها أو مرورها الأول عبر الكبد والرئتين والطحال بواسطة البلعمة المكثفة للمستضدات في تلك الأجهزة بواسطة الخلايا البلعمية المتواجدة فيها . المستضد الدائب لا تتم إزالة بسرعة بسبب بطئ احتساءه بواسطة الخلايا (pinocytic up take by cells) ولكن إذا ما تجمع أو تكدس (Aggregation) المستضد فأن إزالة تتم بشكل أسرع ، مما يدل علي أن حجم المستضد مهمة في عملية البلعمة والاحتساء بواسطة الخلايا.
المرحلة الثانية The second phase :
وهي المرحلة التي تتم فيها عملية هدم تحللي وإزالة تدريجية (gradual catabolic degradation and removal process) وهذه المرحلة تستغرق فترة من 4 إلى 7 أيام وهي تمثل عملية تحليل أنزيمي تدريجي وهضم للمستضد (gradual enzymatic hydrolysis and digestion of the antigen) ، تحديد زمن هذه الفترة ينظم بواسطة القدرة الأنزيمية للعائل . وفي حالة فشل العائل في إنتاج الأجسام المضادة فأن هذه المرحلة قد تمتد إلى عدة أسابيع وتكون هي المرحلة الأخيرة في إزالة المستضد .
المرحلة الثالثة The third phase :
في المرحلة النهائية لأزالت المستضد ، مرة أخرى هناك سرعة في الإزالة وهذه المرحلة في بعض الأحيان تسمي مرحلة الإزالة بالتقطيع أو التجزئة وهي نتيجة تكون أجسام مضادة نوعية جديدة (أي أجسام مضادة نوعية تكونت كاستجابة من الجهاز المناعي ضد المستضد الغريب الذي تم حقنة) تتحد مع المستضد مما يؤدي إلى تنشيط عملية البلعمة والهضم والإزالة للمستضد . الإزالة الكاملة للمستضد من جسم العائل ربما تستغرق عدة شهور أو حتى عدة سنوات .
فرط الحساسية (الحساسية) Hypersensitivity
تفاعلات فرط الحساسية هي استجابة مناعية غير مناسبة أو مبالغ فيها تؤدي إلى تخريب النسيج وليس إلى التمنيع ، وفي الغالب تكون هذة الاستجابة المناعية ضد مواد غير ضارة للصحة . الاستجابة المناعية الناتجة عن تفاعلات فرط الحساسية إذا كانت موجهه نحو مكونات (مستضدات) جسم العائل تؤدي إلى تكوين مناعة ذاتية (autoimmunity) والتي تؤدي إلى حدوث أمراض المناعة الذاتية (autoimmune diseases) .
Allergy is the inappropriate and harmful response of the immune system to harmless substance (الحساسية هي استجابة غير مناسبة من الجهاز المناعي ضد مواد غير ضارة).
تم تقسيم تفاعلات فرط الحساسية إلى أربعة أنواع من قبل كومبس وجيل (Coomb`s and Gell) في سنة 1963 إفرنجي وذلك علي النحو التالي :-
1- تفاعلات النوع الأول أو التأقي Type I Hypersensitivity or anaphylaxis
2- تفاعلات النوع الثاني لفرط الحساسية (النمط السام للخلايا) Type II Hypersensitivity or Cytotoxic Type .
3-تفاعلات النوع الثالث (فرط الحساسية المتوسط للمركب المناعي) Type II Hypersensitivity or Immune Complex Reaction .
4- تفاعلات النوع الرابع (فرط الحساسية الأجل أو المتأخر) Type IV Hypersensitivity or Delayed Hypersensitivity.
1- تفاعلات النوع الأول أو التأق Type I Hypersensitivity or Anaphylaxis :-
هذا النوع من تفاعلات فرط الحساسية هو اكثر الأنواع الأربع شيوعا من حيث المعرفة بين عامة الناس وعند ذكر كلمة حساسية فهي في الغالب لتعبير عن أحد مظاهر تفاعلات النوع الأول لفرط الحساسية . تحدث هذة التفاعلات عند الأفراد الذين لديهم تحسس مسبق أو استعداد وراثي للمستضد المسبب والذي يعرف باسم اللآرجين (allergen) ، والذي يكون في الغالب من مواد غير ضارة بالصحة. أن أهم المواد المسببة لتفاعلات فرط الحساسية من النوع الأول هي؛ حبوب اللقاح ، الغبار المنزلي ، الروائح العطرية المختلفة ، بعض أنواع الاغدية كالسمك والبيض واللبن وبعض أنواع الأدوية كالبنسلين ، المركبات البروتينية كالأمصال والهرمونات وسموم الحشرات وحتى الحيوانات وخصوصا الأليفة منها ؛ كالقطط والكلاب . يتم التعرض لهذه المواد المحسسة عبر الاستنشاق (inhalation) والامتصاص (absorption) ، أو عبر الجهاز الهضمي من خلال الفم أو بالتماس المباشر مع الجلد وعن طريق الحقن .
أن المسبب لتفاعلات فرط الحساسية ليس المواد المذكورة أعلاه في حد ذاتها وإنما بعض مكونات هذة المواد هي التي تؤدي إلى أحداث تفاعلات فرط الحساسية .
الغبار المنزلي House dust :- يتكون الغبار المنزلي من مواد عديدة منها العفن (Moulds) وقشر الجلد (Skin scales) الجاف المتساقط من البشر والحيوانات ولكن المكون الغالب للغبار المنزلي هو السوس (العت) المجهري أو ما يعرف بسوس الغبار المنزلي (House dust mites) ومخلفاته. والذي يعتبر اكبر مصدر للحساسية في العديد من دول العالم ، وخصوصا النوع الذي يتغذى علي قشر الجلد المتساقط من البشر والذي يتواجد بنسبة عالية في غرف النوم .
تفاعلات النوع الأول من فرط الحساسية يعرف أيضا باسم فرط الحساسية الفوري (Immediate hypersensitivity) وسميت هكذا لان التفاعل يحدث خلال دقائق من حدوث التماس مع المستضد المسبب .
يُصاب بهذا النوع من فرط الحساسية في الغالب الأفراد الذين لذيهم ميل طبيعي أو استعداد وراثي لهذا النوع من الحساسية ويطلق علي مثل هؤلاء الأفراد اسم اتوبك (Atopic) وتسمي الحالة بـAtopy ، حيث أن هذا النوع من فرط الحساسية يمكن وراثته من الأبوين إذا كان الاثنان أو أحدهما يعاني من هذا النوع من تفاعلات فرط التحسس . ومن ابرز مسبباته غبار حبوب اللقاح والغبار المنزلي وبعض الأدوية كالبنسلين وبعض الاغدية .
*العناصر الأساسية في أحداث تفاعلات فرط الحساسية من النوع الأول هي :-
1-اللآرجين (The allergen) .
2- الأجسام المضادة من نوع IgE (IgE antibody) .
3-الخلايا الصارية ~ الخلايا القعدة (The mast cells ~ basophils) .
4-الوسائط (Mediators).مثل الـHistamine وLeukotriene (أو ما يعرف بـSRSA) وProstaglandin و Kinin.
طريقة حدوث التفاعل :-عند التعرض لأول مرة لأي من هذة المواد (اللارجينات Allergens) فأن ذلك يؤدي إلى تنبيه الجهاز المناعي علي إنتاج (تكوين) كمية كبيرة من الأجسام المضادة النوعية (من نوع IgE) لذلك الآرجين مـن نوع IgE ترتبط من المنطقة Fc مع مستقبلاتها الموجودة علي اسطح الخلايا الصارية (Mast cells) في الأنسجة والبازوفيل (Basophils) في الدورة الدموية غالبا ، وفي هذة المرحلة لا تشاهد أي تغيرات شكلية في تركيب الخلايا الصارية المرتبط بها الجسم المضاد E (IgE) ولكن عند التعرض لذات اللآرجين لمرة أخرى ، فأن اللآرجين يرتبط مع الأجسام المضادة من نوع IgE المرتبطة بأسطح الخلايا الصارية أو القعدة مما يثير أو يقدح (Triggered) الخلايا الصارية أو البازوفيل مما يؤدي إلى مسخ أو خسف حبيبات تلك الخلايا (Degranulation) مؤدياً بها إلى إطلاق المواد الأمينية الموسعة للأوعية الدموية الشعيرية أو ما يعرف بالوسائط الخاصة بتفاعلات الحساسية (The Mediators of Allergic Response) (مثل الهستامين واللوكريتين) ، ويتم ذلك بانتقال الحبيبات إلى سطح الخلية ثم تتسرب عبر السطح إلى خارج الخلية. هذة المواد تسبب ظهور اعرض تفاعلات فرط الحساسية المتمثلة في توسع الأوعية الدموية الشعيرية وزيادة نفاديتها للبلازما فتسبب الاحمرار والودمة ، وكذلك تسبب تقلص (ضيق) القصبات الهوائية والعضلات الملساء وزيادة الإفرازات المخاطية ، وتجدب الخلايا الحمضية (Eosinophils) إلى منطقة التفاعل (التحسس) والتي تقوم بعملية التهام وتحطيم المعقدات المناعية المتكونة (أي الناتجة من تفاعلات فرط الحساسية) . كل هذة الحوادث (التفاعلات) تؤدي إلى حدوث أعراض شديدة تتمثل في أعراض الصدمة مثل انخفاض ضغط الدم وطفح جلدي وإغماء . حدة وموقع هذة الأعراض وخطورتها يعتمد علي عدد وموقع وجود الخلايا الصارية المنشطة وهذه بدورها تعتمد علي كمية المستضد (اللآرجين) وطريق دخوله إلى جسم العائل وإذا كانت المواد الأمينية الموسعة لذات الدموية الشعيرية المفرزة تفوق قدرة جسم العائل علي تحملها فأن الحالة قد تؤدي إلى الوفاة .
الوسائط الخاصة بتفاعلات الحساسية The Mediators of Allergic Response
1- الهستامين Histamine
هو عبارة عن أمين وزنة الجزيء حوالي 111 دالتون يوجد في حبيبات سيتوبلازم الخلايا الصارية والبازوفيل و بدرجة اقل في الصفائح الدموية في بعض الحيوانات. للهستامين تأثيرات خاصة في الالتهاب حيت يعمل علي زيادة نفادية الأوعية الدموية وتقلص القصيبات الهوائية والعضلات الملساء ويزيد من إفرازات الغدد المخاطية في المسالك الهوائية .
عمل الهستامين يبدأ في خلال دقيقة إلى دقيقتين من بداية حصول التفاعل ويستمر حوالي 10 دقائق تم يتحطم في البلازما والأنسجة بفعل أنزيمات الهستامين (histaminases) ، والهستامين هو المسؤول عن ظهور أعراض حمي القش والشري وتقلص القصيبات الهوائية مؤديا إلى ضيق التنفس .
2- العامل الجاذب للخلايا الحمضية الخاصة بالتأق Chemotactic factor of Anaphylaxis Eosinophil :-
هو عبارة عن ببتيد حامضي وزنة الجزيء حوالي 500 دالتون يفرز بعد حدوث تفاعل المستضد (اللارجين) مع الجسم المضاد المرتبط من المنطقة Fc مع الخلايا الصارية أو البازوفيل . هذا العامل ينتج مسبقا ويخزن في الحبيبات وعند إفرازه يسبب جلب أعداد كبيرة من الخلايا الحمضية (Eosinophils) إلى مكان التفاعل حيت تعمل علي التهام وإزالة المعقد المناعي المتكون من المستضد والجسم المضاد .
3- الوسائط المنتجة حديثا (الوسائط الثانوية) Newly synthesized mediators :-
ومخلفاته تشمل كل من الأتي:-
ا-الماد البطيئة التفاعل الخاص بالتأقSlow reactive substance of anaphylaxis (SRS-A) أو التي سميت حديثا باسم اللوكرترينات (Leukotrenes , C4, D4, E4) ولهذه المادة قابلية عالية علي تقليص القصيبات الهوائية ولذلك فهي تعتبر المسبب الرئيسي للربو .
ب- البرستوكلاندين Postaglandins
هذة المادة منتشرة بكثرة في الأنسجة وهي التي تسبب تقلص العضلات الملساء وتوسيع الأوعية الدموية الشعيرية وزيادة نفاديتها . ومخلفاته المواد هي المسؤولة عن أعراض الشري (Wheal) واحمرار الجلد .
** تكون أعراض تفاعلات النوع الأول أما موضعية كما في حالات الشري وحمي الكلا (حمي القش) أو تكون الأعراض علي شكل إفرازات أنفية وعطاش وحكة في الأنف والعين أو علي شكل هجمات متكررة من ضيق التنفس ومخاط كما في الربو أو تكون الأعراض عامة علي شكل ضيق تنفس ناتج عن تشنج قصبي وهبوط في ضغط الدم نتيجة الاحتقان الوعائي .
** هذا النوع من تفاعلات فرط التحسس يمكن نقلة من شخص محسس إلى آخر سليم عن طريق المصل وبالتالي ينصح الأفراد الذين يعانون من أي من ظواهر تفاعلات النوع الأول من فرط التحسس بعدم التبرع بالدم خصوصا التبرع بالدم الكامل لأنه مثل هؤلاء الأفراد كمية الأجسام المضادة من نوع IgE تكون مرتفعة عندهم .
من الأمثلة علي ظواهر تفاعلات النوع الأول لفرط التحسس الأتي :-
1- حمي القش (الكلا) (Hay Fever) تكون الأعراض فيها علي شكل حكة واحمرار في الأنف والعيون مع كثرة العطاش وزيادة في الإفرازات الأنفية .
2- الشري Urtricariar rash or nettle تكون الأعراض فيها موضعية علي شكل حكة وانتفاخ في الجلد .
3- الربو (Asthma) هو من اشد واخطر ظواهر تفاعلات النوع الأول لفرط الحساسية ، حيث تكون الأعراض فيه علي شكل هجمات متكررة من ضيق التنفس مع صفير (Wheezing) (أو ازيز ربوي) بسبب ضيق القصبات الهوائية وسعال مصحوب ببلغم وهبوط في ضغط الدم .
4- الحكة (Eczema) تكون الأعراض فيها علي شكل طفح جلدي غالبا ما يكون شديد في طيات الجلد مثل خلف الركبة وفي مقدمة المرفق وقد يغطي جسم الطفل في حالة الإصابة الشديدة وهذا قد يشاهد أيضا عند البالغين في شكل طفح جلدي يغطي أجزاء عديدة من الجسم كاليدين والقدمين .
أنواع الغرس Type of Transplants
1-الغرس الخلوي cellular transplants: وهذا النوع يشمل حالات
ا- نقل الدم Blood transfusion.
ب- نقل خلايا نخاع العظم Bone marrow cells.
ج- نقل الخلايا الليمفاوية Lymphocyte transfer in experimental animals.
د- نقل الخلايا الجدعية (stem cells)
2- غرس الأنسجة Tissue transplantation : وهذا يشمل الأتي :
ا- زراعة الجلد ب- زراعة القرنية
3- غرس الأعضاء : وهذا في العادة يشمل الأتي:
ا- زراعة الكلية ب- زراعة القلب
زراعة الكبد ، الرئة والبنكرياس.
4- الجنين The fetus as nature’s homograft : يعتبر الجنين غرس نمطي طبيعي في جسم ألام.
الرقع التي لا ترفض Graft that are not rejected :
هناك بعض الرقع التي إذا ما تم غرسها في الجسم لا يتم رفضها و هذة تشمل الأتي:-
1- المواقع المختارة Privileged sites:
هناك بعض المواقع في الجسم تفتقد إلى وصول التصفية الليمفية الجيدة أليها مثل الجزء الداخلي من العين(anterior chamber of the eye) والقرنية (the cornea) والمخ ( the brain ) ومع أن المستضدات المؤخودة من هذة الرقع قد تصل إلى الأنسجة الليمفاوية ألا أن الخلايا الليمفاوية التائية السامة للخلايا والمؤثرة لا تتمكن من الوصول إلى تلك الرقع لذا فأن مثل هذة الرقع تبقي ولا يتم رفضها ولهذا السبب تعتبر عمليات زراعة (غرس) القرنية المخالفة من الرقع الناجحة في الإنسان.
2- المني(الحيامن = الحيونات المنوية) Sperm:
يستطيع المني بنجاح ولمرات عدة من اختراق السبيل التناسلي للمرأة (reproductive tract) بدون أن يحدث فيها استجابة مناعية وهذا عائد إلى وجود بعض المكونات في السائل المنوي تعتبر مواد مثبطة للمناعة (immunosuppressive) ، حيث أن البلازما المنوية (seminal plasma) تعتبر من المثبطات المناعية والحيامن التي تتعرض لهذا السائل تكون غير مستمنعة (أي غير مولدة للمناعة) حتى بعد الغسل. سائل البروستاتة (prostatic fluid) يعتبر أيضا أحد مكونات البلازما المنوية المثبطة للمناعة ، كما أنة يكبح (يثبط) التحلل الدموي بواسطة المتمم (inhibits complement-mediated hemolysis).
3- الحمل Pregnancy :
نظراً إلى أن الجنين والمشيمة يحملا مستضدات أبوية فهي تعتبر غرس نمطي (مخالف) (allograft) في رحم ألام ولكن علي الرغم من ذلك لا يتم رفضه وينجح في التكون والحفاظ علي نفسه أثناء فترة الحمل علي الرغم من الاختلاف الكبير في أنسجة التوافق النسيجي ، ألا أن الكيفية التي يتم بها ذلك غير مفهومة بشكل جلي ومن المعروف أن الرحم لا يعتبر من المواقع المختارة في الجسم (أي من المواقع المعزولة عن الجهاز المناعي) وفي بعض الحالات تكون ألام أجسام مضادة ضد مستضدات الكريات الحمراء لجنينها (كما في حالة الاختلاف في عامل الريسس (Rhesus factor) بين ألام والجنين) مؤدية إلى تحطم كريات الدم الحمراء للجنين في الرحم أثناء الحمل في الإنسان وبعد الولادة في الثدييات الأخرى بعد تجرعها للباء (colostrum). ولقد وجد بأن التحطم المناعي للجنين يتم منعة بواسطة جملة من الفعاليات المشتركة للعديد من الآليات النوعية والغير نوعية المثبطة للمناعة وهذه تشمل الآتي:-
ا- الجنين الملتقط لا يحمل مستضدات التوافق النسيجي من الصنف الأول أو الثاني وعندما تتكون المشيمة فأن الجنين تتم حمايته من الجهاز المناعي للأم بواسطة الأرومة المغذية (trophoblast) (الأرومة المغذية هي ذلك الجزء من المشيمة الملامس جدا لأنسجة ألام) والأرومة المغذية تحتوي علي تركيز منخفض جداً من مستضدات التوافق النسيجي وتغطي أيضا بطبقة من الزلال المخاطي الغير مناعي.
ب- الجنين يعتبر مصدر لعوامل التثبيط المناعي مثل هرمون الاسترادول (estradiol) والبروجسترون (progesterone ) وربما أيضا هرمون الـHuman chorionic gonadotrophin ، وكذلك البروتين الرئيسي (-fetoprotein) في مصل الجنين يعمل كمثبط للمناعة ، بحكم قدرته علي تحفيز وظيفة الخلايا المثبطة (stimulate suppressor cell function). إضافة إلى وجود عدداً من البروتينات السكرية التي تتواجد أثناء فترة الحمل ومنها الـ2-macroglobulin وانترفيرون المشيمة. كما أن السائل الامنيوني (Amniotic) يحتوي علي كميات كبيرة من الدهون الفسفورية المثبطة للمناعة.
جـ- كاستجابة للمستضدات الجنينية يتم إنتاج الأجسام المضادة الحاصر (Blocking antibodies) والخلايا المثبطة والتي تتداخل مع الاستجابة المناعية المضادة للجنين من ألام. حيث تقوم الأجسام المضادة الحاصره بتغطية خلايا المشيمة فتمنع بذلك تحطيمها بواسطة الليمفاويات التائية للأم. هذة الأجسام المضادة يمكن تحريرها ثانية من خلايا المشيمة وقد وجد أنها يمكنها أن تثبط التفاعلات المناعية الخلوية الأخرى المضادة لمستضدات ألام مثل رفض الرقع ولقد وصف أن عدم وجود الأجسام المضادة الحاصره تؤدي إلى بعض حالات الإجهاض المتكرر في النساء.
تفاعلات الطعم الموجة ضد العائل ( الثوى ) Graft Veruses Host Reaction ( GVHR) :
ويقصد بها هي انه عند غرس عضو إنسان مناعته سليمة في إنسان آخر ذي مناعة ضعيفة فأن الليمفاويات التائية في العضو المزروع (المنقول) تتعرف علي مستضدات أنسجة المضيف (المستلم ، خصوصاً إذا كان العضو المنقول غير متوافق مع المستلم) ، حينها تقوم الليمفاويات التائية بمهاجمة خلايا المستلم وتبدأ تفاعلات (استجابة) مناعية متوسطة بالخلايا في أنسجة العائل تكون أعراضها السريرية في صورة اضطرابات كبدية وطفح جلدي مشابه لطفح الحصبة واسهالات ويبداء الضمور العام وقد تنتهي الحالة بالوفاة وتكون هذة الأحداث اشد ما تكون في حالات زراعة نخاع العظم وبوجه اقل في زراعة الكبد وأجزاء من الأمعاء والجلد وقليلاً ما تشاهد في حالات زراعة القلب والكلية لأن هذة الأعضاء عادتاً تغسل جيداً قبل النقل لتخلص من اكبر كمية ممكنة من الخلايا التائية ولهذا تتطلب عملية نقل نخاع العظم تطابقاً نسيجيا مطلق لتفادي تفاعلات الطعم الموجة ضد العائل.
تفاعلات رفض الطعم Rejection Reactions :
قد يحدث رفض للطعم بآليات تختلف عن بعضها في الطريقة والزمان ، ولكن وصفت ثلاث أنواع مهمة هي:
1- الرفض فوق الحاد hyperacute rejection والذي يحدث في حالة عدم وجود تطابق بين الفصائل الدموية (ABO)، أو جود أجسام مضادة مسبقة تتفاعل مع مستضدات المعطي. تكون نوع التفاعلات من النوع الخلطى أي بين الأجسام المضادة في المعطي مع مستضدات المستلم في وجود عناصر المتمم.
2- الرفض الحاد المتسارع acute or accelerated rejection:يحدث هذا النوع بعد 10 – 30 يوم من بعد عملية الزرع ويعتقد أن هذا النوع من الرفض يكون بسبب المناعة الخلوية المتوسطة بالخلايا، حيث أن الخلايا التائية للمستلم تتعرف علي وتتحسس لبعض مستضدات العضو المزروع فتبداء في سلسلة التفعل المناعي.
3- الرفض المزمن chronic rejection يمكن أن يحدث هذا الرفض بتوسط الخلايا (استجابة خلوية) أو بتوسط المناعة الخلطية أو بكلتيهما ويحدث هذا النوع من الرفض بشكل بطئ وقد يستغرق عدة شهور أو عدة سنوات.
الالتهاب Inflammation
هو عبارة عن استجابة مناعية طبيعية لا نوعية تقوم بها الأنسجة الحية كرد فعل تجاه الإصابة (الجرح injury) والتهيج (irritation).تعتبر هذة الاستجابة آلية حماية هامة وحيوية جداً لأن بواسطتها العوامل الدفاعية مثل الجلوبيولينات المناعية والمتمم والخلايا الأكولة تستطيع الوصول إلي موقع غزو الجراثيم أو النسيج المعطوب والالتهاب . يعتبر اساسياً وضرورياً لبقاء الكائن الحي على قيد الحياة. فبدون الالتهاب لا تكون هناك حماية ضد تأثيرات المنبهات الخارجية المؤدية ولا عملية إصلاح النسيج المتضرر، ولكن في بعض الأحيان يبتعد الالتهاب عن الدفاع عن الجسم ويكون اكثر ضررا للجسم من العامل الضار نفسه والذي سبب التهاب. والأمثلة على ذلك تفاعلات فرط الحساسية وتفاعلات الذاتية المناعة الالتهاب.
تكون استجابة الالتهاب في صورة مجموعة من التفاعلات الدموية والوعائية والخلوية والكيماوية التي تحدث عبر مرحلتين ؛ الأولى تسمي المرحلة الوعائية (Vascular phase) والمرحلة الثانية تسمي المرحلة الخلوية (Cellular phase). وينتج عن تلك التفاعلات الأعراض التقليدية (the classic signs of inflammation) التالية في موقع الالتهاب:
1- آلـــم Pain : بسبب توسع الأوعية الدموية وتهيج الأطراف العصبية بسبب زيادة الضغط عليها وإطلاق حامض اللكتيك (lactic acid) والهستامين من الخلايا العدلة (neutrophils) والخلايا الحبيبية الأخرى المشتركة في تفاعل الالتهاب.
2- احمرار Redness : بسبب توسع الأوعية الدموية الشعيرية وتجمع الدم في موقع الإصابة.
3- تورم Swelling : بسبب زيادة النفاذية الناتجة عن زيادة المسافات بين خلايا الأوعية الدموية الغشائية مما يؤدي إلى تسرب البلازما وتجمع السوائل ، وكذلك بسبب تجمع كمية كبيرة من الدم في النسيج الملتهب.
4- حرارة Heat : بسبب توسع الأوعية الدموية وزيادة تدفق الدم.
5- العجز الوظيفي للعضو أو النسيج المصاب أحيانا Sometime loss of function ، بسبب التورم و تحطم النسيج
تصنيف الالتهاب :
يصنف التهاب بطرق مختلفة. فهو قد يكون يصنف على انه معتدلاً (mild) أو شديد (sever) وذلك حسب طبيعة المادة المثيرة للالتهاب، أو يصنف بالاستناد إلى فترة امتداد الالتهاب (duration) فهو قد يكون حاد (acute) أو تحت حاد (subacute) أو مزمن (chronic) . وفترة امتداد الالتهاب تحددها شدة المثير .
المرحلة الوعائية ( Vascular phase ):
تحدث مباشرة بعد حدوث الإصابة (الجرح) وذلك من خلال إطلاق نواتج المرحلة الفـورية (immediate phase product) وهي الهستامين (Histamine) من الخلايا الصارية (البدينة) (mast cells) والبازوفيل (Basophils) والسروتينين (serotonin) مـن الصفائح الدموية. هذه المواد الكيماوية تطلق خلال دقائق مـن حدوث الجرح مؤدية إلى توسع الأوعية الدموية (Vasodilatation) في موقع الإصابة (إعطاء) مما يؤدي إلي زيادة تدفق الدم إلى موقع الالتهاب مكـونا زيادة في كمية الدم في موقع الالتهاب (Hyperemia) ، مسبب احمرار وحرارة وهذا يؤدي إلى رشح (leakage) محتويات سوائل البلازما إلى خارج الأوعية الدموية الشعيرية ، تكون نتيجتها حصول تورم وآلم. هذه التأثيرات قد تطول بإطلاق نواتج المرحلة المتأخرة (late phase product) التي تحدث خلال 6 إلى 12 ساعة بعد حدوث الجرح المسبب للالتهاب وتشمل هذة النواتج نواتج جهاز المتمم C3a و C4a و C5a والكينين (Kinin) والتجلط (Coagulation) والجراثيم و النتروفيل (Neutrophils) ووحيدات النواة (Monocytes) والليمفاويات (Lymphocytes).
سائل النتح Exudate :
أن أهم خصائص المميزة الالتهاب الحاد هي تكون النتح (exudate). ويتكون سائل النتح كنتيجة لزيادة النفاذية عند حدوث التهاب الحاد مما يسمح بخروج بروتينات البلازما عبر جداران الأوعية الدموية .
يتكون سائل النتح تقريبا من ذات المكونات البروتينية الموجودة في البلازما بالإضافة إلى الخلايا الميتة في موقع إعطاء ومسببات إعطاء (الجراثيم والخلايا الميتة في موقع الإصابة والكريات البيضاء). ولذا فأن سائل النتح يحتوي علي مواد مضادة للبكتريا (antibacterial substances) وأجسام مضادة نوعية وأدوية (drugs) ومضادات حيوية (antibiotic) أن وجدت في البلازما إذا كان قد تناول الشخص أي منها.يعتبر سائل النتح مضادات للجراثيم تساعد علي قتل أو الحد من نشاط الجراثيم المسببة للالتهاب وتعمل كذلك على تخفيف حدة التهيج الناتج عن المواد الكيماوية أو سموم الجراثيم (dilute any irritating chemicals and bacterial toxins) في موقع الإصابة أيضا الفيبرونجين (fibrinogen) الموجود بالنتح يتحول إلى فيبرين (fibrin) بواسطة تأثير ترمبوبلاستين الأكولة (by the action of tissue thromboplastins) مؤديا إلى تكون جلطة الفيبرين (fibrin clot) مشكلة شبكة رفيعة (fine network) تعمل كاعازل لمنع دخول الجراثيم إلى المنطقة الملتهبة والمساعدة في عملية البلعمة.
المرحلة الخلوية Cellular phase :
زيادة تدفق الدم وفقدان السوائل الوعائية (البلازما) يؤدي إلى حدوث الاستجابة الخلوية للالتهاب وتشترك فيها كريات الدم الحمراء من خلال تكدسها (stacks = rouleax) في وسط الوعاء الدموي المصاب وفي هذا الأثناء تباشر الكريات البيضاء الهجرة نحو موقع الالتهاب وتتجمع وتلتصق بجدار الأوعية الدموية تم تتسلل إلى خارج الوعاء الدموي عبر خلاياه الغشائية. تجدب الكريات البيضاء نحو موقع الالتهاب بواسطة (الانجذاب الكيميائي Chemotaxis) نواتج الجراثيم أو جهاز المتمم أو مخلفات الخلايا المحطمة أو الملتهبة.
الخلايا العدلة (Neutrophils) تبداء حركتها نحو موقع الالتهاب بعد حوالي من 30 إلى 60 دقيقة بعد حدوث الجرح وتكون هي الخلايا الرئيسية والسائدة في موقع الالتهاب الحاد وبسبب سرعة هجرتها فأنها تصل أولا إلى موقع الالتهاب وتبداء في التهام الجراثيم وبقايا الخلايا المتحطمة أو المعقدات المناعية.
تعتبر كمية العوامل الجاذبة في موقع التهاب هي التي تحدد زمن استمرار هجرة الخلايا العدلة إلى موقع الإصابة والتي قد تستمر لفترة من 24 إلى 48 ساعة. الأنزيمات الحالة (Lysozyme) التي تفرزها الخلايا العدلة (Neutrophils) تعتبر عوامل جدب للخلايا البيضاء المتعددة النوى الأخرى (Basophils و Eosinophils) إلى موقع الالتهاب ، حيث أن الخلايا القعدة (Eosinophils) تشارك أيضا في التهام الجراثيم وبقايا الخلايا المتحطمة بنسبة اقل ولكنها تقوم في الأساس بتلطيف (Modulate) حدة الاستجابة الناتجة عن الالتهاب من خلال إطلاقها للعوامل المثبطة لبروتينات الالتهاب.
يلي هجرة الخلايا البيضاء متعددة النوى (PMNs) إلى موقع الالتهاب بعد حوالي من 4 إلى 5 ساعات من حدوث الالتهاب هجرة الخلايا وحيدات النواة (البلعميات الكبرى Macrophages) التي تصل ذروتها بعد حوالي من 12 إلى 48 ساعة وهذه الخلايا تعمل أيضا علي التهام وقتل الجراثيم وإزالة بقايا الخلايا الميتة في موقع الالتهاب.
مصير الالتهاب:
1- الشفاء التام وإعادة بناء الأكولة المعطوبة واستعادة الوظيفة الحيوية للجزء المصاب.
2- حدوث تليف أو تكون دمل أو تورم حبيبي (Granuloma) بسبب موت الخلايا الملتهبة وبالتالي فقدان الجزء المصاب لوظائفه الحيوية.
3- انتشار المرض أو تحوله إلى مرض مزمن وبالتالي إلى التهاب مزمن.
الروماتزم (مرض ينتشر)
الروماتويد المفصلي للدكتورجهاد طليمات
أستشاري المخ والأعصاب
مرض التهابي يتلف الغشاء الزلالي الذي يربط بين العظام والمفاصل، وهو أحد أهم انواع التهاب المفاصل المسببة للاعاقة
ولم يعرف بعد ما الذي يثير جهاز المناعة فيجعله ينتج مواد تسبب هذا الالتهاب، الذي يمكنه أن يدمر جميع مكونات المفصل.
وفي الروماتويد المفصلي يتحول الغشاء الزلالي الذي يكون عادة املس إلى نسيج خشن محبب يسمى ” السبل ” يغزو تجويف المفصل، يقوم هذا النسيج بعد ذلك بإطلاق إنزيمات تلتهم الغضروف والعظام والأنسجة اللينة، وقد تقصر الاوتار الملتهبة، مما يحد من حركة المفصل ويجعل العظام تلتحم معآ، وإذا حدث تمزق في الاوتار تصبح المحصلة عدم احكام المفصل ومرونته الشديدة.
قد يحدث الروماتويد المفصلي في أي سن، لكنه عادة ما يبدأ بين سني العشرين والخامسة والاربعين، وبرغم أن السبب غير معلوم، فإنه قد تكون هناك رابطة جينية وراثية، فالمرض يصيب عائلات بعينها.
اعراض الروماتويد المفصلي:
الروماتويد المفصلي عادة ما يبدأ خفية على شكل ارهاق ووجع يشبه ما يحدث مع دور الانفلونزا يستمر لعدة اسابيع أو شهور قبل أن يظهر التهاب المفاصل الصريح.
وهو عادة ما يصيب عدة مفاصل ويكون متوازنآ على الجانبين، فيستهدف مفاصل متشابهة على كل من جانبي الجسم، وخاصة مفاصل الاصابع، قاعدة الأصابع، الرسغين، الكوعين، الركبتين، الكاحلين، القدمين.
وقد يكون ألم المفصل مستمرآ، حتى بدون حركة، ومن الشائع أن يشعر المريض بتيبس المفصل الصباحي والذي يستمر لمدة ساعة أو أكثر.
إن الثخانة التي تصيب النسيج المفصلي أو تراكم السائل الزلالي في الركبتين والكوعين والرسغين أو مفاصل الاصابع تجعل المفاصل تبدو منتفخة وحمراء اللون ويشعر المرء بالدفء فيها وتؤلم عند لمسها، وقد تعاني من توهج حالة التهاب حاد في الغشاء الزلالي يستمر من بضعة اسابيع الى عدة شهور ثم يزول، وعندما يقل الالتهاب قد تشعر بأنك أقل إرهاقآ، وأفضل حالآ بصفة عامة.
ويكون التلف أوضح ما يكون في المفاصل، لكن المرض قد يصيب الجسم بالكامل، وخاصة في القلب والرئتين والاوعية الدموية والعينين والعقد الليمفاوية والطحال.
وقد تظهر حبيبات جلدية التهابية عند نقاط الضعف مثلما يحدث عند الكوعين، وعلى امتداد الأوتار أو اسفل اصابع القدم، وهذه النتوءات التي يتراوح حجمها بين حبة البسلة وحبة الجوز الامريكي قد تذهب من تلقاء نفسها.
ومن الأعراض الأخرى الشائعة أيضآ للروماتويد المفصلي الإرهاق والحمى والهزال والانيميا.
ومرضى الروماتويد المفصلي قد تظهر لديهم أيضآ مشكلات في العين من بينها الجفاف والاحمرار والحرقان والحكة الجلدية.
ولا يمكن التنبؤ بخد سير الروماتويد المفصلي، فمنذ البداية وصاعدآ نجد الاعراض تهدأ أحيانآ لتعاود التوهج من جديد بعدها بأسابيع أو شهور، وبين الحين والاخر يحدث هدوء تام للحالة، عادة ما يكون في خلال السنة الاولى.
بالنسبة لبعض الناس – عادة أولئك الذين لم يعالجوا – قد يسبب المرض عجزآ شديدآ خلال بضع سنوات.
خيارات علاج الروماتويد المفصلي:
إذا كنت مصابآ بأعراض الروماتويد المفصلي، فقم بزيارة الطبيب كي يجري تقييمآ شاملآ لحالتك الصحية، وهناك اختبارات دم تظهر في بعض الاحيان وجود بروتين يجري في الدم يسمى عامل الروماتويد، غير أن تشخيص الروماتويد المفصلي لا يمكن تأكيده أو نفيه بناء عى وجود أو غياب عامل الوماتويد أو غيره من اختبارات الدم.
اشعات اكس (أشعة إكس) يمكن أن تظهر وجود تلف بالمفصل مميز للروماتويد المفصلي، برغم أن هذه التغيرات قد لا تظهر في المراحل المبكرة من المرض.
وقد تساعد عملية شفط السائل الزلالي باستخدام إبرة الطبيب على تشخيص الروماتويد المفصلي أكثر مما تساعده مع حالات أخرى مثل الالتهاب العظمي المفصلي أو الإلتهاب المفصلي الناجم عن عدوى.
وأعظم فرصة لشفائك من أعرا ض هذ المرض تتوفر لك إذا ما اتخذت الجانب الايجابي في علاج حالتك، ويشمل ذلك اتباع الخطة العلاجية، والتعرف على أوقات توهج الاعراض والاثار الجانبية للعقاقير والمحافظة على ظائف المفصل بالتمرينات المنتظمة، وقد يحيلك الطبيب إلى اخصائي علاج طبيعي كي يساعدك بـ التمرينات وغيرها من أشكال العلاج، مثل العلاج بالحرارة أو العلاج بالبرودة.
أول العقاقير المستخدمة هي الادوية اللاستيرودية المضادة للالتهاب، وخاصة الاسبرين وبدائل الاسبرين للإقلال من الألم والإلتهاب، فإذا لم تحق هذه الادوية فعالية في العلاج خلال الاسابيع الاولى، فإن أغلب الأطباء يضيفون ادوية تؤثر أو تغير جهاز المناعة، مثل الهيدروكسي كلوروكين أو الميثوتريكسات، وفي الماضي كانت تسعمل هذه الأدوية كملاذ أخير، ومن المعلوم الان أن الجرعات المنخفضة تلك العقاقير التي تؤخذ في اوائل المرض يمكن تحسين العلاج.
توصف كذلك أدوية أخرى معالجة للمرض مضادة للروماتيزم مثل العلاج بالذهب أو البنسيلامين أو السلفاسازلاين، ويفضل أن يكون هذا مبكرآ وأن تؤخذ مجتمعة.
أما عقاقير الكورتيزون فتوصف لعلاج حالات التهيج المفاجئة للأعراض وقد توصف بجرعات منخفضة بشكل يومي لكبح جماح الاعراض، غير أن الاطباء لا ينصحون بالاستعمال المتظم للجرعات المرتفعة تفاديآ لحدوث آثار جانبية خطيرة.
وعندما يحدث تلف أو تشوه شديد بالمفصل، قد يصبح من الضروري إجراء جراحة استعاضة المفصل (استبدال المفصل
فإذا اصبت بالروماتويد المفصلي، فإن من المهم أن تعني بالمسائل التالية:
– الغذاء: برغم عدم وجود غذاء معين لمرض الروماتويد المفصلي، إلا أن بعض الدلائل تشير إلى أن الاعراض قد تقل مع تناول أكثر من مقداري تقديم أسبوعيآ من زيت السمك الغني بالاحماض الدهنية العديدة المشبعة بـ اوميجا 3 والتي توجد في السلمون والماكريل والسردين، وقد يكون من المفيد أيضآ تناول تلك الاحماض الدهنية على شكل كبسولات.
– الرحلة والتمارين: يؤدي المصابون بالروماتويد المفصلي وظائفهم على أفضل نحو إذا أمكنهم ضبط مستوى راحتهم ونشاطاتهم بحيث يتوافق مع شدة المرض، وأثناء نوبات الالتهاب الحادة قد تحتاج إلى 8-10 ساعات من النوم ليلآ علاوة على ساعة من الراحة خلال النهار، وقد تكون الراحة ذات قيمة وقائية كذلك، وبعض الناس يبالغون فيها عنما تبدأ الأعراض في الزوال فيجدون أنفسهم مرهقين، إن بضع فترات من القيلولة القصيرة خلال النهار تمنع الارهاق وتتيح لك انجاز المزيد من العمل، أما عن التريض فإنه قد يساعد على الحفاظ على وظائف المفاصل، ويخفف من التيبس ويقلل من الالم والإرهاق، والتريض كذلك يزيد من قوة العظام، وبصفة عامة من الأفضل أن تحرك مفاصلك عن عدم تحريكها، ومن ثم التوازن بين الراحة والتريض هدف مهم.
– حماية المفاصل وتوفير الطاقة: الافراط في استعمال المفاصل الملتهبة يؤدي إلى الألم والتورم، ويضيف المزيد إلى تلف المفصل ، ويمكن لإخصائي التأهيل المهني أن يعلمك كيف تحافظ على طاقتك وتحمي مفاصلك أثناء أداء المهام اليومية بمزيد من اليسر والسهولة ، وهذه التوصيات يمكنها أن تساعدك في السيطرة على الألم والالتهاب:
– تجنب الاوضاع أو الحركات التي تضع المزيد من الضغوط على المفاصل.
– تجنب البقاء في وضع واحد لمدة طويلة.
– خطط مقدمآ للأنشطة وبسّط حياتك بقدر الامكان، فالضغوط قد تعمل على تفاقم حالة التهاب المفاصل.
– عدّل في منزلك لتجعل الحياة ايسر، فيمكنك تثبيت قضبان للإمساك بها والاستناد عليها عند كل من الدش والبانيو مع استعمال وسائل أخرى مساعدة.
– اطلب المساعدة عند تحتاج إليها.
– الجانب العاطفي من الروماتويد المفصلي:
المصابون بالرماتويد المفصلي غالبآ ما ينتابهم القلق من أن يصبحوا معاقين، وعاجزين عن العمل، أو أن يصبحوا عالة على الآخرين، غير أنه لا يصاب بإعاقة شديدة من جراء هذا المرض سوى نسبة صغيرة للغاية من المصابين به. والاكتئاب أمر شائع بين المصابين بأمراض مزمنة ومن بينها الروماتويد المفصلي. وهناك شكل من أشكال العلاج المعرفي يمكنه تقوية الشعور لدى المريض، مما يخفض من درجة الالتهاب والضغوط العصبية التي يشعر بها.
مزايا ومخاطر عقاقير الكورتيكوسيترويدات لعلاج الروماتويد المفصلي:
تبطيء عقاقير الكورتيكوسيترويدات من معدل تلف عظام اليد لدى المصابين بالروماتويد المفصلي ، غير أنها قد تتسبب أيضآ في اثار جانبية خطيرة مثل هشاشة العظام، وكسور العظام، ونزيف القناة الهضمية، والعدوى الميكروبية أو الكتاراكت، ويستطيع طبيبك مساعدتك في تقييم المخاطر والمنافع التي تعود من وراء العلاج بالكورتيكوسيترويدات.
مزايا ومخاطر الميثوتريكسات لعلاج الروماتويد المفصلي:
لدى مرضى الروماتويد المفصلي، يحقق عقار الميثوتريكسات ارتياحآ كبيرآ للأعراض وابطاء في تلف العظام، وهو يسبب اعراض جانبية مثل الفشل الكبدي والغثيان والفيء والصداع والطفح وقرح الفم.
________________________________________
مقال آخر عن الروماتويد المفصلي
يعد هذا المرض من أخطر الامراض الروماتيزمية التي تصيب الانسان، وتكمن خطورته في حقيقة أننا نجهل اسبابه، وبالتالي طرق علاجه.
وفي دراسة أجراها أحد المراكز البحثية تبين أن هذا المرض يصيب 3% من سكان بريطانيا والولايات المتحدة، وتشكل السيدات نسبة 80% منهم، ومع انه قد ثبت ان معدل الاصابة هونفسه في جميع أنحاء العالم، فإن نسبة الإعاقات الناتجة عن
هذا المرض لوحظ أنها اقل في الأقاليم المعتدلة المناخ عنها في الأقاليم الباردة كدول شمال أوروبا. وغالباً ما تحدث الاصابة في سن الاربعين، لكن يمكن في احيان قليلة ان تظهر في العقد الثامن أو حتى التاسع من حياة الانسان. وتتميز الاصابة في الحالة الاخيرة بأن أعراضها تحدث بصورة حادة. لكنها لا تترك آثارا ضارة أو تسبب إعاقة كما يحدث في الحالات الاخرى التي يظهر فيها المرض مبكراً.
ويصيب هذا المرض عدة مفاصل، لكنه يبدأ في مفصل واحد ثم ينتقل منه لمفاصل أخرى. ومفاصل اليد والقدم هي أول ما يصاب من مفاصل الجسم في 70%من الحالات.
اعراض الالتهاب الروماتويدي المفصلي (الروماتويد المفصلي):
تبدأ أعراض هذا المرض بصورة بطيئة على هيئة آلام وتيبس بالمفاصل المصابة خصوصاً في الصباح، دون حدوث ارتفاع في درجة الحرارة، مع شعور بالشعف وكثرة العرق. وفي نسبة قليلة من الحالات تظهر الاعراض بصورة حادة مع ارتفاع في درجة الحرارة. ويزداد الإحساس بالألم عندما يبدأ المفصل في التورم وتقل حركته ويدركه التيبس.
يتميز هذا المرض بوجود فترات تتحسن فيها الاعراض تتبادل مع فترات أخرى تزداد فيها شدة المرض، وينعكس ذلك على زيادة تيبس المفاصل المصابة وتعرضها بالتالي لتشوهات مختلفة.
تشخيص الالتهاب الروماتويدي المفصلي (التهاب الروماتويد المفصلي
يعتمد التشخيص على ملاحظة أعراض المرض وعلاماته المميزة، كما تجرى بعض الفحوصات والاختبارات المعملية الخاصة للتأكد من دقة التشخيص.
علاج الالتهاب الروماتويدي المفصلي (التهاب الروماتويد المفصلي
يتضمن علاج هذه الحالات ما يلي:
1. العناية بتغذية المريض، وإعطاؤه أدوية مقوية وفيتامينات ومركبات الحديد لعلاج الأنيميا التي تصاحب غالبية هذه الحالات.
2. الالتزام بالراحة وتجنب عوامل الإجهاد.
3. تناول الادوية المضادة للالتهابات، وهي كثيرة ومتنوعة، وقد وجد للادوية المضادة للملاريا وأملاح الذهب بعض الفائدة في علاج هذا المرض.
4. تناول عقار الكورتيزون ولكن بمقادير بسيطة محسوبة ولفترة قصيرة، حيث إنه ضرورة لا غنى عنها في المراحل التي تشتد فيها وطأة المرض.
5. مراعاة وضع المفاصل في الأوضاع المريحة للمريض، وقد يتطلب الامر احيانا الاستعانة بجبائر لتفادي حدوث التشوهات، مع تحريك المفاصل من حين لآخر حتى لايدركها التيبس.
6. التدخل جراحياً في الحالات التي لا تتحسن فيها الاعراض او التشوهات رغم مواظبة المريض على خطوات العلاج السابقة، وذلك بإجراء جراحات مختلفة لإصلاح التشوهات او استئصال الغشاء السينوفي أو تثبيت المفصل او استعواضه بمفاصل صناعية.
مبادئ التلقيح (التمنيع)
مبادئ التلقيح

أولا – تصنيف اللقاحات
هناك نمطان أساسيان من اللقاحات هما اللقاحات الحية المضعفة واللقاحات المعطلة وتختلف مزايا وصفات هاتين المجموعتين وهذه الصفات هي التي تحدد كيفية استخدام اللقاح
يتم إنتاج اللقاحات الحية المضعفة عن طريق تعديل الفيروس أو الجرثوم المحدث للمرض (الشكل البري) في المخبر وهذا يؤدي إلى احتفاظ الفيروس أو الجرثوم الموجود في اللقاح بقدرته على التكاثر والنمو و إنتاج المناعة دون أن يكون قادرا على إحداث المرض عادة
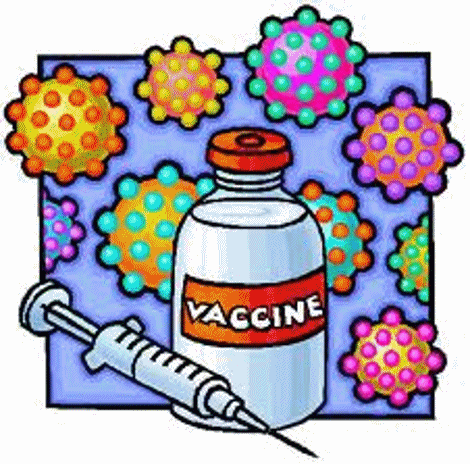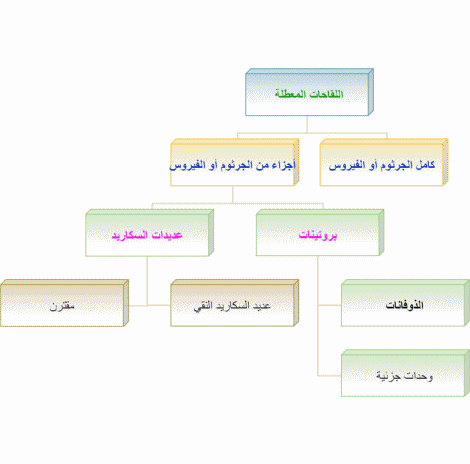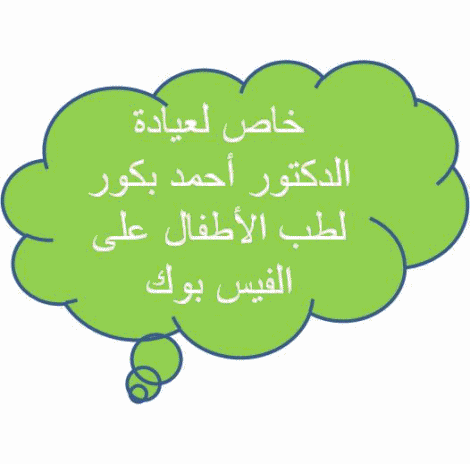
أما اللقاحات المعطلة فقد تكون مكونة من كامل الجرثوم أو الفيروس أو من أي جزء منهما ويكون أساس اللقاحات المجزأة إما بروتينيا أو عديد السكاريد
تشمل الللقاحات التي تحوي على أجزاء بروتينية من الفيروس أو الجرثوم الذوفانات Toxoids (ذيفان الجرثوم المعطل) والوحدات الجزئية أو الجسيمات الفيروسية الجزئية
أما بالنسبة للقاحات التي تحوي عديد السكاريد فمعظمها يتكون من عديد السكاريد النقي الخاص بجدار الجرثوم
وهناك أيضا لقاحات عديدات السكاريد المقترنة التي يرتبط فيها عديد السكاريد كيماويا مع البروتين مما يجعله لقاحا أكثر فعالية
قاعدة عامة : كلما كان اللقاح أكثر شبها بالمرض الطبيعي كانت الاستجابة الطبيعية له أفضل

اللقاحات الحية المضعفة
تشتق من الفيروسات أو الجراثيم المحدثة للمرض (الأشكال البرية) حيث يتم إضعافها في المخبر عن طريق الزرع المتكرر عادة مثلا فيروس لقاح الحصبة المستخدم حاليا كان قد عزل من طفل مصاب بالحصبة عام 1954 وتم إضعاف هذا الفيروس عبر إمراره عبر المزارع النسيجية في سلسلة امتدت 10سنوات قبل أن يتحول من فيروس بري إلى فيروس اللقاح
يجب أن تتكاثر الفيروسات أو الجراثيم الموجودة في اللقاحات الحية المضعفة في جسم الشخص الملقح لكي تحدث الاستجابة المناعية وتعطى عادة كمية صغيرة نسبيا من الجرثوم أو الفيروس المضعف وهذا بدوره يتكاثر وتزداد كميته إلى درجة كافية لإحداث تنبيه للاستجابة المناعية
أي شيء يمكن أن يؤثر على فيروس أو جرثوم اللقاح في الفلاكونة (مثل الضوء أو الحرارة ) أو يتداخل مع تكاثره في الجسم (مثل وجود أضداد جائلة في الدوران ) قد يسبب فشل اللقاح
رغم أن فيروس اللقاح الحي المضعف يتكاثر فإنه لا يسبب المرض عادة كما يحدث مع الفيروس البري وعندما يسبب المرض فإنه يكون عادة أخف بكثير من المرض الطبيعي وندعو ذلك بالارتكاسات الجانبية أو غير المرغوبة
الاستجابة المناعية للقاح الحي المضعف مطابقة عمليا لتلك الناجمة عن الخمج الطبيعي والجهاز المناعي لا يميز بين خمج فيروس اللقاح المضعف والخمج الناجم عن الفيروس البري
بصورة عامة تكون اللقاحات الحية فعالة بعد إعطاء جرعة واحدة منها عدا اللقاحات الحية المضعفة التي تعطى فمويا
قد تسبب اللقاحات الحية المضعفة ارتكاسات شديدة أو مميتة بسبب تكاثر فيروس اللقاح بشكل غير مسيطر عليه وهذا يحدث فقط عند مثبطي المناعة (مثل المصابين بالابيضاض أو الايدز أو الذين يعالجون بأدوية معينة )
قد لا تتطور المناعة الفاعلة بعد إعطاء اللقاح الحي المضعف بسبب تداخل الأضداد الجائلة مع فيروس اللقاح ويمكن للأضداد من أي مصدر كان (المنتقلة عبر المشيمة أو التي تعطى للمريض ) أن تتداخل مع نمو فيروس اللقاح وبالتالي حدوث استجابة ضعيفة أو عدم حدوث استجابة للقاح (فشل اللقاح )ويبدو أن فيروس لقاح الحصبة هو الأكثر تأثرا بالأضداد الجائلة أما فيروسات لقاحي الشلل والروتافيروس فهي الأقل تأثرا
إن اللقاحات الحية المضعفة سهلة العطب وقد تتخرب بالحرارة أو الضوء ولذلك يجب التعامل معها بحذر
اللقاحات الفيروسية الحية المضعفة المتوفرة حاليا هي :
* الحصبة * النكاف * الحصبة الألمانية * الحماق * الحمى الصفراء * الانفلونزا (داخل الأنف )* كذلك لقاح الشلل الفموي لكنه لم يعد متوفرا في الولايات المتحدة * أما لقاح فيروس الروتا المأشوب الحي فما زال مصرحا باستخدامه في الولايات المتحدة لكنه لم يعد يوزع بسبب علاقته مع الانغلاف
تشمل اللقاحات الجرثومية الحية المضعفة : * لقاح الـ BCG * ولقاح الحمى التيفية الفموي

اللقاحات المعطلة
تنتج عن طريق زرع الجرثوم أو الفيروس في أوساط الزرع ثم تعطيله عن طريق الحرارة أو المواد الكيماوية (الفورمالين عادة )
وفي حالة اللقاحات المجزأة فإن الفيروس أو الجرثوم يخضع لمعالجة أخرى لتنقية المكونات المستخدمة في اللقاح فقط ( مثل محفظة عديد السكاريد للمكورات الرئوية )
اللقاحات المعطلة ليست حية وبالتالي لا يمكن أن تتكاثر وتعطى الجرعة الكاملة من المستضد في جرعة اللقاح
لا يمكنها أن تسبب المرض عند مثبطي المناعة
على عكس الحية لا تتأثر بالأضداد الجائلة ولذلك يمكن إعطاؤها حتى لو كانت الأضداد موجودة في الدم (كما هو الحال في فترة الرضاعة أو بعد إعطاء منتجات الدم الحاوية على الأضداد)
تحتاج اللقاحات المعطلة دوما إلى عدة جرعات وبصورة عامة لا تؤدي الجرعة الأولى من اللقاح المعطل إلى إنتاج مناعة واقية لكنها تهيئ الجهاز المناعي وتتطور الاستجابة المناعية الواقية بعد الجرعة الثانية أو الثالثة من اللقاح
على العكس من اللقاحات الحية التي تكون الاستجابة المناعية لها تشابه إلى حد كبير الاستجابة للخمج الطبيعي فإن الاستجابة المناعية للقاحات المعطلة تكون خلطية في معظمها وتنتج مناعة خلوية قليلة
كذلك تفشل اللقاحات المعطلة عادة في إنتاج الأضداد الموضعية على شكل الغلوبيولين المناعي الإفرازي A (IgA ) وهذا يجعلها غير قادرة على حماية المخاطيات ومنع الاستعمار أو الخمج الموضعي بالعامل الممرض رغم قدرتها على الوقاية من الخمج الجهازي
عيار الأضداد الموجهة ضد مستضدات اللقاحات المعطلة تهبط مع الوقت وبالنتيجة تحتاج بعض اللقاحات المعطلة إلى جرعات إضافية دورية لتعزيز مستوى الأضداد
اللقاحات المعطلة المتوفرة حاليا تقتصر على اللقاحات المعطلة التي تحوي كامل الفيروس (الانفلونزا , الشلل , الكلب , التهاب الكبد A)
أما اللقاحات المعطلة التي تحوي كامل الجرثوم (السعال الديكي , الحمى التيفية , الكوليرا , الطاعون ) فلم تعد متوفرة في الولايات المتحدة
وتحوي اللقاحات المجزأة : – وحدات جزئية (التهاب الكبد B , الانفلونزا , السعال الديكي اللاخلوي ) – ذوفانات ( الدفتريا , الكزاز )
لقاح الوحدات الجزئية لداء لايم لم يعد متوفرا في الولايات المتحدة
اللقاح عديد السكاريد
هي نمط فريد من لقاح الوحدات الجزئية المعطلة يتكون من سلسلة طويلة من جزيئات السكر التي تكون المحفظة السطحية لبعض الجراثيم
تتوفر لقاحات عديدات السكاريد النقية ضد ثلاثة أمراض هي- المرض الناجم عن المكورات الرئوية – المرض الناجم عن المكورات السحائية – والسالمونيلا التيفية
أما لقاح المستدميات النزلية النمط b عديد السكاريد النقي فلم يعد متوفرا في الولايات المتحدة
الاستجابة المناعية للقاح عديد السكاريد النقي مستقلة بشكل وصفي عن الخلية التائية أي أن هذه اللقاحات قادرة على تحريض الخلايا البائية دون مساعدة الخلايا التائية المساعدة
إن المستضدات المستقلة عن الخلايا التائية بما فيها لقاحات عديد السكاريد ليست مولدة للمناعة بشكل ثابت عند الأطفال دون عمر السنتين
الأطفال الصغار لا يستجيبون بشكل ثابت للمستضدات عديدات السكاريد بسبب عدم نضج الجهاز المناعي
الجرعات المتكررة لمعظم اللقاحات المعطلة التي تحوي البروتين (الذوفانات أو الوحدات الجزئية ) تؤدي إلى تعزيز مستوى الأضداد في حين لا تؤدي الجرعات المتكررة من لقاحات عديدات السكاريد إلى تعزيز الاستجابة
الأضداد المحرضة باللقاحات عديدات السكاريد ذات فعالية وظيفية أقل من الأضداد المحرضة بالمستضدات البروتينية وسبب ذلك أن الأضداد الناجمة استجابة للقاحات عديدة السكاريد تكون بشكل رئيسي من نوع IgM ولا ينتج إلا كمية قليلة من IgG
وقد اكتشف في أواخر الثمانينات من القرن العشرين أنه يمكن التغلب على المشكلة المذكورة سابقا بعملية تدعى الاقتران حيث أن هذه العملية تغير الاستجابة من استجابة مستقلة عن الخلية التائية إلى استجابة معتمدة عليها مما يزيد القدرة على توليد المناعة عند الرضع وزيادة مستوى الأضداد استجابة للجرعات المتكررة من اللقاح
أول لقاح مقترن كان لقاح المستدميات النزلية النمط b وقد تم ترخيص لقاح المكورات الرئوية المقترن عام 2000 وقد يصبح لقاح المكورات السحائية المقترن متوفرا في المستقبل
جدول التلقيح المعتمد في السعودية

جدول التلقيح المعتمد في سوريا منذ عام 2008
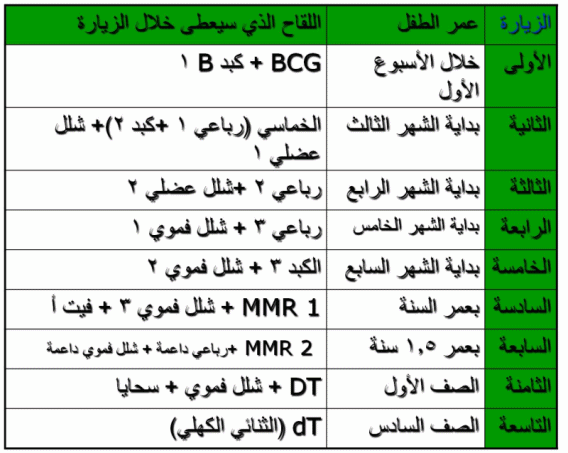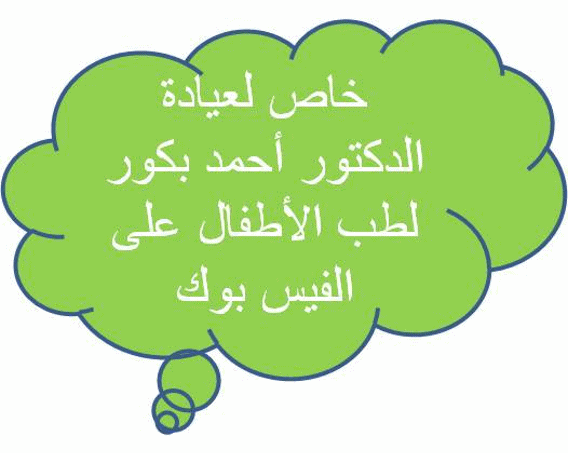
المصدر : عيادة الدكتور أحمد بكور على الفيس بوك
المناعة ضد الجراثيم Immunity to Bacterial Infections
الخلية الجرثومية تتكون من سيتوبلازم يحتوي على كافة المكونات الأساسية لبناء الخلية محاطً بالغشاء الخلوي المحاط بالجدار الخلوي، وفى بعض الأنواع من الجراثيم تكون الجرثومة محاطة بكبسولة (capsular)، كما توجد في بعض أنواع الجراثيم اسواط (flagellar) والبعض الأخر أهداب (pilus). وجود بعض المواد السيتوبلازمية التي تشمل البروتينات النووية والإنزيمات والدهون ومواد أخري إضافة إلى افرازات الجراثيم المختلفة مثل السموم كل هذه المكونات تعتبر في اغلبها مواد مستضدية، ولكن نظراً لوجد هذه المواد السيتوبلازمية في اغلبها داخل الخلية الجرثومية فأنها تعتبر اقل أهمية من الناحية المستضدية من المستضدات الأخرى التي توجد على السطح مثل الجدار الخلوي أو الكبسولة اوالاسواط أو الافرازات السمية من ناحية قدرتها على تحفيز المناعة ضد تلك المستضدات. المناعة المتكونة إما أن تكون مناعة خلطية أو خلوية أو كلتيهما والتي تكون موجهه نحو المستضدات المشار إليها أعلاه.
تكون أمراضية الجراثيم إما بسبب سمومها أو بسبب غزو الجراثيم لأنسجة العائل وتحطيمها.
المناعة التي تحمي العائل ضد الإصابات الجرثومية، تشمل عوامل كثيرة كلها تدخل تحت خط الدفاعات ضد الجراثيم والتي تشمل الحواجز الطبيعية المتمثلة في الجلد الطبيعي والأغشية المخاطية السليمة وكذلك إفراز بعض المواد الخاصة المضادة للجراثيم وغيرها، كما أن لنوع العائل والعوامل الوراثية والعمر لها اثر كبير على قدرة العائل على مقاومة الإصابات الجرثومية، وهناك الاستجابة المناعية النوعية المتمثلة في المناعة الخلطية والخلوية.
أن طبيعة الاستجابة المناعية ضد الجراثيم تعتمد على هل أن الجرثومة من النوع الذي ينمو ويعيش خارج الخلية اى جراثيم خارجية (extracellular) أو من النوع الخلوي إي الذي يعيش داخل الخلية (intracellular). الاستجابة المناعية ضد الجراثيم الخارجية تكون سريعة ومؤثرة ويقوم بها الجهاز المناعي للعائل من خلال تكوين أجسام مضادة اى مناعة خلطية وأيضا السموم التي تفرزها بعض أنواع الجراثيم تكون الاستجابة ضدها تكون خلطية، حيث تقوم الأجسام المضادة المتكونة ضدها على معادلتها وأبطال مفعولها. ومن الضروري يجب أن تكون الاستجابة ضد تلك السموم سريعة وفعالة لتفادي إحداثها ضرر في جسم العائل مثل ما يفعل سم الـClostridium welchii المسبب للموت الغازي (gas gangrene). إذا كانت الجراثيم من النوع الخلوي فهي قد تعيش داخل خلية العائل لفترة طويلة قبل إن تحدث ضدها استجابة مناعية والتي ليست دائماً فعالة وتكون هذه المناعة معتمدة على اللمفاويات التائية اى مناعة خلوية.
عادتا ما تكون الاستجابة المناعية النوعية موجة نحو ثلاثة عناصر جرثومية هي كالتالي:-
1- المناعة ضد الإصابة بالبكتريا السامة Immunity to toxigenic bacterial infections:-
الجراثيم المفرزة للسموم تفرز نوعين من السموم هي السموم الخارجية (exotoxins) والسموم الداخلية (endotoxins)، التي تعتبر مهمة في أمراضية الإصابة ببعض الأنواع من الجراثيم.
ا- السموم الخارجية extoxins:- هي بروتينات مؤدية تفرزها العديد من أنواع الجراثيم (مثل Clostridium tetani و Bacillus species). السموم الخارجية هي من النوع الغير مستقرة في الحرارة إي تتأثر بالحرارة (heat-labile)، ولهذا تستعمل المعالجة بالحرارة لتثبيط نشاطها لتحضير لقاحات منها (مثل لقاح ضد الكزاز (tetanus)، ولكن نظراً لوجود أنواع عديد من الجراثيم التي تفرز أكثر من نوع من السموم (مثل ) يجعل من الصعب تحضير لقاحات ضد مثل تلك السموم.
ب- السموم الداخلية Endotoxins:- جدار الجراثيم السالبة الجرام (gram-negative bacteria) يتكون من معقد من السكريات المتعددة والدهون والبروتينات، وتلك كلها تشكل السموم الداخلية لتلك الأنواع من الجراثيم. وتعود معظم الخاصية السمية إلى المكونات الذهنية في الجدار الخلوي والتي تعرف بالدهن A (Lipid A)، بينما تكون السكريات المتعددة هي المسئولة عن الخاصية المستضدية للمستضد O (اى المستضد الجسدي = somatic antigen)، مثل Brucella abortus و Vibrio cholerae.
الاستجابة المناعية ضد السموم الداخلية يجب إن تكون قادرة على القضاء على الجراثيم الغازية وفى ذات الوقت تكون قادرة على معادلة سمومها.
2- المناعة ضد الجراثيم التي لها كبسولة Immunity to encapsulated bacteria:-
الجراثيم التي تحمل كبسولة من السكريات المتعددة تشكل مشكلة فريدة للجهاز المناعي، لأن كبسولة السكريات المتعددة التي تحملها الجراثيم تثبط عملية البلعمة بواسطة الخلايا الأكولة والكريات البيضاء متعددة النوى أو تثبط عملية الانجذاب الكيميائي لها. تعمل الكبسولة على التداخل مع المستقبلات الموجودة على البلعميات والكريات البيضاء، وبالتالي تمنع التصاقها بالجراثيم، حيث أن عملية البلعمة تتطلب وجود مستقبلات عاملة للمنطقة Fc على الأجسام المضادة ومستقبلات للـC3b، ومن أمثلة الجراثيم التي تحتوي على كبسولة Streptococcus pneumonia، هذا النوع من الجراثيم يصيب الجهاز التنفسي ويسبب ما يسمى بداء الرئة. تعمل الكبسولة في هذه الجراثيم على حمايتها من البلعمة بواسطة البلاعم السنجية (alveulor macrophage) الثابتة في الرئة من خلال تثبيط نشاطها البلعمى، مما يسمح لها بالتكاثر في الرئة Haemophil influenza المسببة التهاب القصبات الهوائية (bronchitis) وداء الرئة (pneumonia) هي الأخر من الجراثيم ذات الكبسولة التي توفر لها الحماية من الخلايا البلعمية (الأكولة) في الرئة. إضافة إلى أنواع عديدة أخري تحمل كبسولة.
يمكن تحضير لقاحات توفر مناعة وقائية مؤثرة ضد هذا النوع من الجراثيم باستخدام لقاحات تحتوي على مستضدات الكبسولة النقية.
3- المناعة ضد الجراثيم الخلوية Immunity to intercellular bacteria:-
هذا النوع من الجراثيم هي من النوع المجبر على العيش داخل خلايا العائل. هذه الجراثيم التي تستطيع التهرب من / أو تجنب الجهاز المناعي للعائل، من خلال غزوها لخلايا العائل والعيش فيها بعيداً عن الجهاز المناعة وهى أيضا قد تغزو بعض الخلايا المناعية ومثلها في ذلك مثل بعض الفطريات والطفيليات، مما يجعل الأجسام المضادة والمتمم غير قادرة على الوصول إليها، كما أن الكريات البيضاء والبلاعم الاخري لا تستطيع تميزها على أنها غريبة. كما أن معظم الجراثيم الخلوية تمتلك وسائل لمقاومة وحماية نفسها من الجهاز المناعي مثل Brucella abortus التي لها جدار مقاوم لتخريب بواسطة الإنزيمات الحالة في البلاعم (phagosome-lysosome)، وCorynebacterium pseudotuberculosis التي يوجد لها جدار خلوي دهني سام للبلعميات.
الجراثيم الخلوية تتم مقومتها من قبل الجهاز المناعي للعائل بواسطة المناعة الخلوية التي تعتبر أساس مقاومة الجراثيم من خلال إنتاج خلايا تائية محسسة وبلعميات منشطة، حيث يتم إبراز مستضدات الجراثيم الخلوية على سطح البلعميات بعد عملية تحضير المستضد بالارتباط مع معقد التوافق النسيجي من الصنف الثاني وفى هذا الإطار البلعميات ترتبط مع الخلايا التائية المحسسة لإنتاج عامل تنشيط البلعميات (macrophage activating factor)، مثل الجاما انترفيرون ن وكل هذه السلسلة المعقدة من الإحداث ضرورية لتكوين مناعة مؤثرة ضد هذا النوع من الجراثيم المرضية.
المناعة النوعية ضد الإصابة بالجراثيم:-
هناك ثلاث آليات أساسية تستطيع بواسطتها الاستجابة المناعية النوعية مقاومة غزو الجراثيم وهى كالتالي:-
1- معادلة (neutralization) السموم والإنزيمات الجرثومية بواسطة الأجسام المضادة.
2- قتل الجراثيم بواسطة الأجسام المضادة والمتمم والإنزيمات الحالة ومضادات الجراثيم في افرازات الجسم وفى البلعميات.
3- إعداد الجراثيم للبلعمة (opsonization)، بواسطة الأجسام المضادة (والمتمم) يؤدي إلى بلعمتها وتحطيمها بواسطة البلعميات.
وسائل مقاومة أو تهرب الجراثيم من الاستجابة المناعية:-
البكتريا مثل كل الطفيليات لا يخدمها موت عائلها أو إزالتها بواسطة جهازه المناعي. ولهذا عادتا ما يكون للجراثيم إلية متطورة تستطيع بواسطتها تجنب أو التهرب من الاستجابة المناعية للعائل. وكما اشيره اعلاة بعض الجراثيم تستطيع حماية نفسها من الجهاز المناعي مثلاً بواسطة الكبسولة (الكبسولة المضادة للبلعمة) (anti-phagocytosis capsule) أو باختيارها لتطفل الخلوي (اى بالعيش داخل خلايا العائل)، وبالتالي تؤخر مهاجمتها من قبل مناعة العائل. بينما تفرز بعض الجراثيم مواد مثبطة لعملية البلعمة بواسطة النتروفيل مثل ما تفعل E. coli و Mycobscterium tuberculosis ، وتستطيع الـS aureus حماية نفسها من خلال إفرازها لسموم مثل ستربتوليسين O (streptolysin O) الذي يعمل على حل خلايا النتروفيل وهناك أنواع أخري من الجراثيم تفرز سموم مضادة للكريات البيضاء والبلعميات.وتوجد جراثيم لها القدرة على تثبيط النشاط المضاد للجراثيم في خلايا العائل فمثلا الصبغة الصفراء (carotenoid) المسئولة عن لون الـS. aureus يمكنها إن تخمد singlet oxygen وبذلك يجعل الـS. aureus مقاومة للـrespiratory burst ، كما أن الـS. aureus تستطيع تثبيط البلعمة بواسطة البروتين A (protein A) الموجود على سطحها حيث أن البروتين يرتبط مع المنطقة Fc للجسم المضاد IgG ، مما يمنعه من الارتباط مع المستقبلات الخاصة به الموجودة على البلعميات وطاهيات الجراثيم .
أنواع المناعة Types of Immunity
وسائل الجسم لمقاومة مسببات المرض لا تنحصر في نوع واحد مـن الفاعليات المناعية بل أنها تشمل وسائل مناعية عديدة متخصصة وغير متخصصة (specific and non-specific) وعلى هذا الأساس فقد صنفت المناعة بشكل عام إلي نوعين هما :- المناعة التي تتواجد مع الكائن الحي مند الولادة وتتطور وتنضج مع تطور نمو ونضوج الكائن الحي ويسمي هذا النوع من المناعة بالمناعة الطبيعية (الفطرية أو اللانوعية) والنوع الثاني هي المناعة التي يكتسبها الفرد بعد تعرضه بشكل طبيعي أو اصطناعي للمواد الغريبة المسببة للأمراض أو نقل مواد مناعية جاهزة (مثل الأجسام المضادة) له بشكل طبيعي أو اصطناعي ويسمي هذا النوع من المناعة بالمناعة المكتسبة أو المناعة النوعية .
– المناعة الطبيعية (الفطرية أو اللانوعية) Natural (Innate or non-specific) immunity :-
وهي المناعة التي يرثها الكائن الحي من والدية وتنمو وتتطور فاعليتها بشكل طبيعي مع تطور حياة الإنسان ويبدأ عملها مند الولادة في مقاومة غزو الأجسام الغريبة والميكروبات الضارة ولا تعتمد آليتها علي عوامل خلـوية أو خلطيه محددة ولا تحتاج إلى التعرف النوعي علي الأحياء الدقيقة أو الأجسام الغريبة الغازية للقيام بدورها المناعي وتعمل هذة المناعة بذات الطريقة في كل مرة يتعرض فيها الجسم للمهاجمة من قبل الأجسام الغريبة من جديد ويمكن تعريف المناعة الطبيعية على أنها عبارة عن خطوط دفاعية ميكانيكية وكيميائية وخلوية ؛ هذا النوع من المناعة يتكون من آلاتي :-
1- الحواجز الميكانيكية Mechanical barriers :-
وهي الحواجز المعيقه لدخول الأحياء الدقيقة الضارة والأجسام الغريبة وهي تمثل خط الدفاع الأول عن الجسم حيث تقوم بمنع التصاق أو اختراق الجراثيم والفيروسات أو المواد الغريبة للجلد أو الأغشية، كما تقوم هذه الوسائل الميكانيكية بإزالة أو منع نمو أو تكاثر الأحياء الدقيقة التي تعلق أو تلتصق بالجلد أو الأغشية، وهذه الحواجز تشمل آلاتي :-
ا- الجلد : الجلد السليم والخالي من العطب أو الجروح يعتبر عائق ميكانيكي لدخول الأحياء الدقيقة والأجسام الغريبة إلى الجسم حيث يعمل الجلد كغلاف واقي للجسم ويعتبر الجلد خط الدفاع الأول في جسم العائل لوقايته من الإصابة .
ب- الشعر: يعتبر أيضا عائق ميكانيكي يعمل علي منع التصاق الأحياء الدقيقة بالجلد والأغشية المخاطية .
ج- الأغشية المخاطية: التي توجد في كل أعضاء الجسم التي لها اتصال خارجي، مثل الجهاز الهضمي والتنفسي ، تفرز مخاط يمنع التصاق الأجسام الغريبة والجراثيم بخلايا تلك الأعضاء .
د- الخلايا الظاهرية ذات الأهداب (ciliated epithelial cells) : كالتي تتواجد في الجهاز التنفسي تقوم بحجز وإخراج الجراثيم والجزيئات الصلبة العالقة بالطبقة المخاطية بواسطة حركة الأهداب .
هـ- الإفرازات الحمضية والأنزيمية للماعده، لها تأثير مضاد للعديد من الأحياء الدقيقة التي قد تدخل عبر الفم.
و- اللعاب والعرق لهما دور منظف .
ز-الدموع : تعمل علي إزالة الجزيئات الصلبة والأجسام الغريبة التي قد تدخل للعين ، كما أن الأنزيمات التي تفرزها العين لها القدرة علي القضاء علي العديد من الميكروبات .
س- المسالك البولية ، حيث تساعد في إزالة الميكروبات وغيرها أثناء عملية التبول .
ك- العطس، السعال، القيء، والإسهال، كلها لها دور منظف من خلال طرد الجراثيم والأجسام الغريبة إلى خارج الجسم .
ك- المهبل : إفرازات المهبل في النساء تعتبر وسط حمضي غير ملائم لنمو الجراثيم .
م-المطاعمة أو النبت الطبيعي (Normal flora) ، تقوم الجراثيم المطاعمة المتواجدة في الأمعاء بالتقليل من احتمال التصاق ونمو الجراثيم الممرضة (الضارة) بالغشاء المعوي.
2-الحواجز الكيميائية The chemical barriers:-
العديد من سوائل وإفرازات الجسم الكيميائية لها دور دفاعي وتعتبر من الخطوط الدفاعية الأولية للمناعة الطبيعية في الجسم وهذه السوائل والإفرازات تشمل آلاتي :-
ا- التعرق ونواتج الغدة الزهمية (perspiration and product of sabucious gland) تعطي سطح الجلد وسط حامضي مثبط لنمو العديد من الجراثيم ، مثل حامض اللكتيك (lactic acid) الذي هو من محتويات العرق وكذلك أنزيم الليزوزيم (Lysozyme) ، كما أن الأحماض الدهنية التي يفرزها الجلد تكون سامة لأنواع عديدة من الأحياء الدقيقة الضارة .
ب- الدمع يحتوي علي أنزيم الليزوزيم القاتل للجراثيم خصوصا الجراثيم الموجبة الجرام (gram +ve) .
ج- حامض الهيدروكلوريك ، الذي تفرزه الماعده له قدرة علي قتل غالبية الجراثيم التي قد تدخلها عبر الفم .
د- البول : يعتبر وسط حمضي مثبط لنمو العديد من الجراثيم، كذلك وجود بعض الأنزيمات في البول تعمل على التخلص من الجراثيم التي قد توجد في المجاري البولية.
هـ- الأنزيمات الحالة (الليزوزيم) Lysozyme:- وهي عبارة عن أنزيمات (خمائر) حالة تفرز من قبل الكثير من الخلايا في الجسم (مثل كريات الدم البيضاء وخلايا الأغشية المخاطية وخلايا الطحال …الخ)، كما أنها توجد في العديد من إفرازات الجسم مثل الدمع والعرق والبول وإفرازات الغدة اللعابية وسوائل الجسم الأخرى عدا سائل النخاع الشوكي ، وهذه الأنزيمات لها تأثير مضاد للجراثيم حيث تعمل علي شق السكر الموجود في الجدار الخلوي للجرثومة بنوعيها الموجبة والسالبة الصبغة مما يؤدي إلى تحلل الجدار وبالتالي موت الجرثومة .
و- الإفرازات المهبلية في النساء ، تحمي الجهاز التناسلي للمرأة لاحتوائها علي أحماض تقضي علي الميكروبات .
س- السيتوكينات Cytokines :- الجهاز المناعي يؤدي وظائفه من خلال تفاعل تبادلي (تأثير أو فعل متبادل interactions) معقد بين مختلف الخلايا ، هذا التأثير المتبادل أما أن يحدث من خلال الاتصال المباشر بين الخلية والخلية (by direct cell to cell contact) أو بتوسط pharmacological agents ، واهم هذة الوسائط الببتيدات المتعددة التي تسمي السيتوكينات (cytokines).
السيتوكينات تعتبر وسيط هام لدفاعات العائل ضد الإصابة (infection) والجروح (injury) ، وضد الالتهاب الحاد أو المزمن (acute and chronic inflammation) وغالباً ما تقوم ذات السيتوكينات بالتوسط في الحالتين. السيتوكينات أيضا مهمة في التوسط لنمو وتمايز الخلايا الجدعية (stem cells) التي تنشاء عنها خلايا الـmyeloid cells (الخلايا النخاعية) والـlymphoid cells (الخلايا الليمفية) الناضجة .
السيتوكينات تفرزها خلايا الجهاز المنتج للخلايا الدموية (haematopoietic system) وتعمل عليها مثل الليمفاويات (lymphocytes) والبلعميات (macrophages) ، ولكن أيضا يمكن أن تنتجها خلايا أخرى من غير خلايا الجهاز المناعي وتعمل عليها .
السيتوكينات هي عبارة عن بروتينات تفرزها العديد من الخلايا المناعية المنشطة وكذلك الخلايا الغير المناعية و تعمل كساعي خلوي بروتيني (intercellular messenger proteins) ، تؤثر علي أداء الجهاز المناعي لوظائفه وتربطة مع أجهزة فسيلوجية أخرى في الجسم .
تشمل السيتوكينات كل من الانترليوكينات من 1 إلى 12 (interleukins 1 to 12 ~ ~ IL-1 to IL- 12) ، الانترفيرونات (interferons ~ IFNs) ، العوامل المحفزة لمجاميع الخلايا (colony-stimulating factors ~ CSFs) ، وعامل النخر الورمي الفا وبيتا (tumor-necrosis factors and ) ، بالإضافة إلى عدد من عوامل منظمات النمو الأخرى، حيث تقوم هذة السيتوكينات بتحفيز أو بتثبيط وتنظيم عمل خلايا أخرى من الجهاز المناعي ، كما أنها تؤثر في عمل أعضاء أخرى مختلفة بالجسم . وتعد هذة الجزيئات منظمات حاسمة لكل مظهر من مظاهر مناعة الفقاريات ، مع ملاحظة بأن السيتوكينات التي تفرزها وحيدات النواة تسمى مونوكينات والتي تفرزها الخلايا الليمفاوية تسمي اللمفوكينات .
Cytokines secreted by monocytes are called monokines, and those from lymphocytes are called lymphokines.
الانترفيرونات Interferons = IFN:- هي مجموعة من البروتينات أو البروتينات السكرية (Glycoproteins) تفرزها الخلايا المصابة بالفيروس وتعمل على حماية الخلايا المجاورة من الإصابة بالفيروس (أي الخلايا الأخرى الغير مصابة بالفيروس) من خلال منع استنساخ الفيروس داخل الخلية (أي بمنع تصنيع الرنا RNA الفيروسي). الانترفيرون ليس له علاقة بالفيروس وإنما يفرز كرد فعل من قبل الخلايا المصابة ضد الفيروس ، كما أن للانترفيرون دور في التنظيم المناعي مثل كبح تنشيط الليمفاويات البائية (inhibition of B-cell activation) وتنشيط النشاط السمي الخلوي للخلايا القاتلة الطبيعية (enhancement of the cytotoxic activity of natural Killer cells) ، كمـا أن له القدرة علي منع نمو الطفيليات الخلوية ، وأيضا الإصابة بالطفيليات الخلوية (intercellular parasites) (مثل الـchlamydiae والـrickettsiae) والبروتوزوا (protozoa) مثل الـToxoplasma والجراثيم (مثل الـstreptococci والـstaphylococci) ومنتجات الجراثيم السمية (endotoxins) ، كما أن هذة كلها تؤدي إلى تنشيط إنتاج الانترفيرون من قبل الخلايا. الانترفيرون لا يتأثر بالحرارة أو الحموضة وتم التعرف علي العديد من أنواع الانترفيرونات أهمها الآتي :-
* انترفيرون آلفا (IFN-):- يفرز بواسطة الخلايا البيضاء ( بالذات البلعميات ووحيدات النواة) ويعمل علي تنشيط مضادات الفيروسات وتنشيط الخلايا القاتلة الطبيعية (NK) ، ويطلق أيضا علي IFN- انترفيرون الخلايا البيضاء (Leukocyte interferon). للـIFN- نشاط مضاد للفيروسات .
* انترفيرون بيتا (IFN-) :- يفرز هذا الانترفيرون من قبل الخلايا الـfibroblasts cells والخلايا الطاهرية (epithelial cells) والبلاعم الكبيرة (Macrophage). الدور الأساسي للـIFN- هو النشاط المضـاد للفيروسات (antiviral activity) ، الـIFN- يطلـق علية ايضا اسم epithelial-fibroblast interferon أو fibroepithilial interferon .
* انترفيرون جاما (IFN-):- وهو الانترفيرون الرئيسي المفرز من قبل الليمفاويات وتعتبر الليمفاويات التائية المفرز الرئيسي له، ودورة الأساسي يتمثل في التنظيم المناعي . ويطلق علي الـIFN- أيضا اسم الانترفيرون المناعي (immune interferon) .
** يعرف كل من الـIFN- والـIFN- بالانترفيرون نوع 1 (Type I interferon) ويعرف الانترفيرون IFN- باسم انترفيرون نوع 2 (Type II interferon) .
* عامل النخر الورمي Tumor Necrosis Factor (TNF) :- يعتبر عامل النخر الورمي وسيط أساسي في استجابة العائل ضد البكتريا السالبة الصبغة, وربما يلعب أدوار أخرى في الاستجابة ضد الإصابة بأحياء دقيقة أخرى. المصدر الرئيسي لعامل النخر الورمي هو السكر المتعدد الدهني لوحيدات النوي البلعمية المنشطة (الاكوله) (Lipopolysaccharid-activated mononuclear phagocyte) والليمفاويات التائية المنشطة بواسطة المستضد (antigen-stimulated T cell) والخـلايا القاتلة الطبيعية المنشطة (activated NK). كما أن الخلايا الصارية المنشطة (activated mast cells) هي الأخرى لها القدرة علي إفراز هذا العامل .
* الانترلوكينات (IL) Interleukins :- هي أحد أفراد عائلة السيتوكينات الواسعة، وتعمل هذة الانترلوكينات كأداة اتصال أو ربط بين خلايا الجهاز المناعي المختلفة ومن جهة أخرى بين الجهاز المناعي وخلايا الجسم الأخرى ، بالإضافة إلى مساعدة الجهاز المناعة في أداء وظيفته الدفاعية .
Interleukins provide a means of communication among cells within the immune system and between the immune system and other cells of the body.
توجد عدة انترلوكينات عرفت بأرقام عربية متسلسلة مثل الانترلوكين-1 (IL-1), الانترلوكين-2 (IL-2) …الخ. تقوم بإنتاجها العديد من الخلايا المناعية مثل البلعميات و الليمفاويات البائية التي تنتج الانترلوكين-1 (IL-1)، و الليمفاويات التائية التي تنتج كل من الانترلوكين-2 (IL-2) و 3 و 4 .
ك- البروبيردينات Properdins :- هي عبارة عن بروتينات ( جاما جلوبيولين ) تعمل علي تنشيط المسلك البديل لنظام المتمم مؤديا إلى قتل الجراثيم التي تغزو الجسم بواسطة تفعيل نظام المتمم .
ل- الـBetalysin :- مصل العديد من الحيوانات بما فيها الإنسان يحتوي علي مادة لها نشاط مضادة للبكتريا (Antibacterial activity) ، تعرف باسم Betalysin و التي تفرز من قبل الصفائح الدموية أتناء عملية التجلط (Released by platelets during coagulation) . ولهذه المادة دور دفاعي في إطار المناعة الطبيعية للجسم ضد البكتريا الممرضة وبالذات البكتريا الموجبة الجرام (gram- positive bacteria) باستثناء الـ streptococci.
م-الأجسام المضادة الطبيعية Natural antibodies :-
الأجسام المضادة الطبيعية هي تلك الأجسام المضادة الموجودة في الجسم دون تعرض مسبق للمستضد النوعي لها. وتوجد عدة فرضيات تشرح سبب وجودها منها العوامل الوراثية، والتصالب مع مستضدات لها نفس الأماكن المحددة (epitops) لتكون هذة الأجسام المضادة ، أو أن المستضدات قد دخلت إلى الجسم دون أدراك العائل لها و أدت إلى تكون هذة الأجسام المضادة .
ع- بروتينات الطور الحاد Acute phase proteins :
هي مجموعة من البروتينات تصنع غالباً في الكبد مثل الـ1-antitripsin, و C-Reactive protein ، وceroloplsma ، والفيبرينوجين …الخ . هذا البروتينات ترتفع نسبها بشكل حاد في المصل عند حدوث التهابات حادة أو حادث للأنسجة بأي سبب كان، كالإصابة بالجراثيم أو نتيجة أي عطب أخر في الأنسجة.
Acute phase proteins :- Proteins synthesized by the liver whose level in serum rises rapidly in response to acute inflammation and tissue damage. .
ن- جهاز المتمم ( أو المكمل) Complement system : وهي أحد المكونات الطبيعية للبلازما وتتكون من كثر من 20 بروتين أو بروتين سكري لها دورة أساسي وفعال في دفاعات الجسم المختلفة ضد غزو الميكروبات والأجسام الغريبة .
3- الحواجز أو العوامل الخلوية المشتركة في المناعة الطبيعية (المناعة الخلوية الطبيعية) :-
كريات الدم البيضاء بأنواعها المختلفة تعتبر هي الحواجز الخلوية في دفاعات الكائن الحي وتعتبر هي خط الدفاع الثاني والأساسي في الجسم حيث أنه في كثير من الأحيان تستطيع الكثير من الميكروبات من اختراق الحواجز الميكانيكية والكيميائية لجسم العائل وهنا تتدخل الحواجز الخلوية بأنواعها منع ضرر تلك الميكروبات الغازية من خلال القضاء عليها بواسطة البلعمة أو من خلال إنتاج الجلوبيولينات النوعية (الخلايا الليمفاوية) المضادة لتلك الميكروبات الغازية وإنتاج عوامل تساهم بشكل فعال في مقاومة الجسم ضد الميكروبات هي الغريبة الأخرى الضارة .
تعتبر الكريات البيضاء له الوحدات المتحركة للجهاز المناعي بأنواعها الجسم حيث تستطيع الانتقال إلى مختلف أنحاء الجسم لتأدية وظائفها الدفاعية ، والقيمة الحقيقية للكريات البيضاء تكمن فأن اغلبها تنتقل إلى موقع الإصابة أو تواجد الميكروبات هي الغريبة الضارة وتعمل على تحطيمها بواسطة عملية تدعى البلعمة . وتقوم بعملية البلعمة كل الكريات البيضاء بقدرات مختلفة ( تعتبر الخلايا العدلة ووحيدات النواة الأهم والأكثر فاعلية في عملية البلعمة بالمقارنة بالخلايا الحمضة والقاعدة) عدا الليمفاويات التي يتمثل دورها القيام أحداث المناعة المكتسبة بنوعية الخلطي والخلوي .
المناعة الخلطية : الجزء الأول
1ـ: Introduction المدخل ـ
للتذكير ،إذا صببنا مصل حيوان محصن في أسطوانة تحتوي على الأناتوكسين المثبت على مسحوق عاطل ، فإن السائل الذي ينفذ عبر الأسطوانة لا يحمل المصل الواقي دليل على حصول ارتباط وهو ما يعرف بالإستجابة المناعية الخلطية للأضداد Anticorps بالمستضدات Antigènes . و تحدث الإستجابة الخلطية عن طريق الأضداد المفرزة من طرف الخلايا البلازمية ،(Fig.1) . و لذلك يمكن الإستفادة منها و نقلها من كائن لآخر عن طريق نقل مصل الدم دون بقية مكوناته . وتدعى المناعة التي تنتج عن حقن الإنسان بمستحضرات مناعية إستخلصت من مصل إنسان آخر أو مصل حيوانات بالمناعة السلبية Immunité passive كما هو في حالة الترياق Antitoxin والمصل المضاد Antiserum .
2 ـ طبيعة الأضداد :
هي جزيئات من البروتينات السكرية الكروية الموجودة في الدم وتدعى بالجلوبيلينات المناعية Immunoglobulines ويرمز لها بالرمزIg ويتم انتاجها من طرف الخلايا اللمفاوية البائية Lymphocytes B بعد تمايزها إلى خلايا بلازمية كاستجابة للمستضد بعد التعرف عليه من طرف الضد الخاص به .
2 ـ1ـ التركيب الجزيئي للجلوبين المناعي :
تشترك الغلوبيلينات المناعية في البنية الأساسية ، وتأخذ هذه البنية شكل حرفY أو K . ويتكون الضد من اتحاد نوعين من السلاسل عديدة البيبتيد Polypeptides المعروفتان بالسلاسل الثقيلة و السلاسل الخفيفة وفي كل ضد توجد سلسلتان ثقيلتان متماثلتان وسلسلتان خفيفتان متماثلتان تربط بينهما جسور ثنائية الكبريت Ponts désulfure ولكل سلسلة نهايتان إحداهما أمينية NH2 ـ والأخرى كربوكسيلية COOH ـ . وتمثل الأشكال Fig 5 ، 4 ، 3 ، 2 البنية الجزيئية للغلوبيلين المناعي .
وبناء على ترتيب الأحماض الأمينية في كل سلسلة بالقرب من الطرف الحامل لمجموعة ، فقد تم التعرف على خمسة أنماط من السلاسل الثقيلة في مصل الإنسان الكربوكسيل ¯COO ويسمى الغلوبيلين المناعي تبعا لنوع السلسلة الثقيلة الموجودة فيه . وعليه يمكن تمثيل صفوف الغلوبيلينات المناعية ب (Tab.1 , Fig.6) .
(Tab.1) صفوف الغلوبيلينات المناعية
الغلوبيلين المناعي
السلسلة الثقيلة
IgM
Mu ميو μ
IgG
Delta دلتاY
IgA
Alpha الفاα
IgD
Gamma جاماδ
IgE
Epsilon ابسلونξ
و يكون ترتيب الأحماض الأمينية بالقرب من الطرف المحتوى على مجموعة الكربوكسيل ثابتا في السلاسل الثقيلة في حين يكون هذا التركيب مختلفا بشكل كبير عند الطرف المحتوى على مجموعة (NH2) للسلاسل الثقيلة. و عليه تدعى هذه المنطقة بالمنطقة المتغيرة Région variable . وبالنسبة للسلاسل الخفيفة تقسم كذلك تبعا لترتيب الأحماض الأمينية بالقرب من الطرف المحتوى على مجموعة الكربوكسيل و يوجد نوعان من السلاسل الخفيفة هما lambda L و Kappa k مع أي من السلاسل الثقيلة و لا يمكن أن نجد النوعين (L) أو(k) معا في جلوبيلين مناعي واحد مصنع من نفس الخلية اللمفاوية . وعليه يصطنع الفرد نمطين لغلوبيلين مناعيين ، يختلفان من الناحية الثابتة للسلسلة الخفيفة ، وأن حوالي نصف جزيئات الغلوبيلين المناعي يحتوي على سلاسل خفيفة (L) و يحتوي النصف الآخر على سلاسل خفيفة (k) .
2 ـ 2 ـ المنطقة الثابتة والمنطقة المتغيرة :
في كل من السلاسل الثقيلة والخفيفة تترتب الأحماض الأمينية بشكل ثابت في الناحية القريبة من الطرف المحتوى على مجموعة الكربوكسيل وتدعى تلك المنطقة بالمنطقة الثابتة Region constante وتحتوي على حوالي 100 حمض أميني بالنسبة للسلسلة القصيرة و حوالي 320 بالنسبة للسلسلة الطويلة . أما الجزء الباقي من السلسلتين فيتألف من أحماض أمينية غير ثابتة أي متغيرة الترتيب . و تحتوي على حوالي 120 حمضا أمينيا بالنسبة للسلسلة الطويلة و110 بالنسبة للسلسلة الخفيفة وتدعى بالمنطقة المتغيرة (Pasternek ,1986 ) Région variable . و يمكن تمثيل الأحماض الأمينية في كل من السلسلة الخفيفة و الثقيلة ب (Fig.7) .
2 ـ 3 ـ المجالات Domaines :
تقسم السلاسل الثقيلة إلى المجالات الآتية :
ـ مجال المنطقة المتغيرة VHوتحتوي على 120 حمضا أمينيا.
ـ المجال الأول الثابت CH1
ـ المجال الثاني الثابت CH2 المنطقة الثابتة تحتوي على 320 حمضا أمينيا
ـ المجال الثالث الثابت CH3
و تقسم السلسلة الخفيفة إلى المجالات الآتية :
ـ المجال المتغير VL وتحتوي على حوالي 110 حمضا أمينيا .
ـ المجال الثابث CL وتحتوي على حوالي 100 حمضا أمينيا .
وعليه فإن المنطقة المتغيرة للغلوبيلين تتألف من المجالين (VL+VH)2 في حين تتألف المنطقة الثابتة من القطاعات (CH3+CH2+CH1)+CL وأصبح معروفا أن مجالات كل منطقة تقوم بالوظائف التالية :
ـ تقوم المجالات VH+VL بالارتباط بالمستضد .
ـ يقوم CH3, CH2 بالارتباط بالمتمم .
ـ يقوم CH3 بالارتباط بمستقبلات البلعميات و وحيدات النواة .
ـ يقوم CH3, CH2 بالارتباط بمستقبلات خلايا المشيمة و خلايا وحيدات النواة والخلايا
القاتلة .(أرحاب و آخرون 1993 ) .
2 ـ 4 ـ منطقة المفصلة:
في مركز (وسط) كل سلسلة ثقيلة (منطقة اتصال المجالين CH2,CH1 ) يوجد بين هذين المجالين، يتكون البروتين غالبا من بقايا السيستين و البرولين Cysteine,Proline حيث تقوم بقايا السيستين بتكوين الروابط ثنائية الكبريت في حين تعمل بقايا البرولين على المحافظة على الشكل الكروي و تدعى منطقة الإتصال هذه بمنطقة المفصلة ، وهي تمد السلسلة الخفيفة بخصائص الغلوبيلينات المناعية حيث أنها تسمح بمرونة flexibilité ذراعي الشكل Y كما أنها تسهل عملية فتح وغلق الذراعين للتكيف والمستضد .
2 ـ 5 ـ قطعة Fab و Fc:
تم التعرف على هذه القطع عند تحليل الغلوبيلينات بواسطة الأنزيمات المحللة للبروتين Protease مثل ال Papain وال Pepsin
حيث أحدث الPapain إنشطار الغلوبيلين إلى :
1-قطعتين متماثلتين : تتألف كل منهما من سلسلة خفيفة مرتبطة بنصف سلسلة ثقيلة ، ولوحظ أن هاتين القطعتين قادرتان على الارتباط بالمستضد و لذلك سميتا بقطعة الارتباط بالمستضد ( Fragment antigene binding (Fab.
2- قطعة منفردة : تتألفCH3 ,CH2 السلسلة الثقيلة و قد لوحظ أنها سهلة التبلور وعليه سميت بالقطعة المتبلورة (FC) Fragment cristallisable وهي ليست قادرة على الارتباط بالمستضد في بداية التفاعل بعد ارتباط Fab بالمستضد مثل حالة ADCC حيث ترتبط Fc بمستقبلاتها على الخلايا القاتلة الطبيعية و بذلك فهو يركز جزيء الغلوبيلين على الخلايا القاتلة لتقوم هذه الأخيرة بتحطيم الجزيء الغريب .
3- وظائف الضد :
يقوم الضد بالعديد من الوظائف نذكر منها مايلي :
1.3 ـ تعديل سمية المستضد Neutralisation de l’antigène
يؤدي ارتباط الضد بالمستضد إلى منع تأثير السم، و يعتبر IgG أحسن ضد يقوم بإزالة المواد السامة في الدم مثل حالة سم العقارب و الثعابين و حالة الكزازTetanos ونظرا لقدرته على تعديل بعض السموم،عادة بتثبيط موقعها الفعال ، ونظرا لطول مدة نصف الحياة بالمقارنة مع الغلوبيلينات الأخرى فإن IgG هو المفضل في التمنيع السلبيImmunisation passive ويمكن تمثيل تعديل السمية ب (Fig.8) .
Opsonisation الطهو ـ 2 . 3 :
يعني تحضير المستضد لإبتلاعه من طرف البالعات وفي هذه الحالة يرتبط الضد بالمستضد ،وبما أن بعض البالعات الكبيرة و متعددة النوى تحمل مستقبلات غشائية خاصة بالجزء Fc فإن هذا الجزء يرتبط بهذه المستقبلات على غشاء تلك الخلايا ، ومن ثم يبدأ الغشاء في الإحاطة بالجسم الغريب إلى أن يصبح هذا الجسم ( البكتريا مثلا) داخل الخلية البالعة ليتم هدمه . و بهذا يكون الضد قد .ساعد على عملية البلعمة .و يمكن تمثيل عملية الطهو ب (Figs.9.10) .
3.3 ـ تنشيط المتمم Activation du complement :
إن ارتباط الضد بالمستضد يحرر موقع التثبيت للمتمم المحمول على جزيئة الضد و هو ما يعمل على تنشيط المتمم و إجراء التفاعلات التي تؤدي إلى تحليل الجسم الغريب . مثلا يستطيع IgG أن ينشط جهاز المتمم و ذلك بتحرير العديد من المواد النشيطة بيولوجيا والتي تؤدي إلى تحليل المستضد بعد ارتباطه بالضد . بعض هذه المواد تعتبر كمواد طاهية Opsoninesحيث تربط المستضد و الخلايا البالعة التي تحمل مستقبلات نوعية لهذه المواد الطاهية و بذلك تدعم بلع المستضد . كما أن بعض هذه المواد لها تأثير كيميائي حيث يقوم بجذب الخلايا البالعة نحو مركز التفاعل بين الضد و المستضد . ويمكن تمثيل تنشيط المتممة ب (Fig.11) .
: ADCC 4.3الوساطة بربط المستضد بالخلايا ذات السمية
يلعب IgG دورا هاما في الوساطة بين المستضد بالخلايا السامة القاتلة حيث يرتبط بالضد من جهة ومع هذه الخلايا القاتلة من جهة أخرى لتقوم هذه الأخيرة بالقضاء على المستضد. وفي هذه الحالة يرتبط المستضد يكون فيها المستضد إما مكروبا أو خلية سرطانية فإنFabفي حين يرتبط الجزء Fc بمستقبلاته النوعية التي توجد على غشاء الخلية القاتلة الطبيعية (NK) ، وبذلك يكون الضد قد عزز عملية ارتباط الخلايا القاتلة بالمستضد (هدفها) . و تقوم الخلايا القاتلة هذه بإفراز مواد سامة للقضاء على الأضداد .
Diversité des anticorps 4تنوع الأضداد
كما هو معلوم فإن كل ضد يحمل العديد من المحددات ، و يتم التعرف على كل منها من طرف ضد معين (خاص) .كما أنه يوجد الملايين من محددات المستضد ،و عليه فإن العضوية قادرة على تكوين الملايين من الأضداد المختلفة و منها فقط يطرح التساؤل فيما إذ كان المجين Génome قد يحتوي على عدد كبير من المورثات . و قد أظهرت الدراسات أن العضوية تنتج عددا من أنماط الأضداد أعلى بكثير من عدد المورثات في المجين . هذا ، ويمكن توضيح ذلك التنوع في الأضداد بتعضى المورثات في الضد وكذلك بمستويات إعادة الترتيب كمايلي :
1.4- تعضى مورثات الضد :
مهما كان نمط الضد فإنه يملك بنية قاعدية مشكلة من أربع سلاسل متعددة البيبتيد كما سبق ذكره . و تظهر المورثات المشفرة لهذه الأجزاء المختلفة للبروتين عدة خصائص مهمة .
إن مورثات الأضداد ليست جميعها على نفس الصبغي ، فالمورثات المشفرة للسلاسل الثقيلة محمولة على الصبغي 14 في حين تحمل المورثات المشفرة للسلاسل الخفيفة على الصبغين 2 و 22 . و يمكن تمثيل توضع مورثات الضد على الصبغيين الثاني و الرابع عشر ب (Fig.12) .
و يوجد لكل نمط من سلسلتي الغلوبيلينات المناعية (الخفيفة أو الثقيلة) تجمع من المورثات المفصولة عن بعضها البعض على جزيئ الحمض الريبي منقوص الأكسيجسن ADN . وكل تجمع من هذه المورثات يحتوي على مورثات V (مشفرة للمناطق المتغيرة) وعلى مورثات C (المشفرة للمناطق الثابتة) . ومن المعلوم أنه يوجد جينان مشفران للمناطق المتغيرة في السلاسل الخفيفة هما جينا J et V في حين توجد ثلاثة جينات مشفرة للمناطق المتغيرة في السلاسل الثقيلة هي جينات D,J,V .وعلى سبيل المثال هذه بعض المعطيات العددية : يوجد حوالي 150 مورثة V و5 مورثات J بالنسبة للسلاسل الخفيفة أما بالنسبة للسلاسل الطويلة فيوجد 80 مورثة V و50 مورثة D و6 مورثات J . وتمثل هذه الأرقام الحد الأدنى بالنسبة لعدد جزيئات الأجسام المضادة المحتملة .
وكخلاصة إن جينات الأضداد مقطعة إلى كسر صغيرة مبعثرة تبعثرا واسعا في أرجاء المجين Genome. و يوجد في أضداد الثدييات نوعان من السلاسل الخفيفة . فللسلسلة الخفيفة لمدا في الفأر جينان V يشفران معظم المنطقة المتغيرة ، وأربع جينات C تشفر المنطقة الثابتة . وتوجد في كل جين صعدا قطعة صغيرة من DNA أطلق عليها الحرف J (من كلمة الوصل Joining ) ، وتحدد هذه القطعة نوعية بقية المنطقة المتغيرة . وكل جين من نوع V يستطيع التواجد من أي زوج من جينات J و C .و يوجد للسلسلة الخفيفة كابا بضع مئات من القطع V وأربع قطع من J وجين واحد من C . أما جينات السلسلة الثقيلة فتماثل جينات السلسلة الخفيفة ، فيما عدا أن Vدنا المنطقة المتغيرة مقسم إلى أجزاء أصغر : فبالإضافة إلى قطع V و J توجد حوالي 20 قطعة من D (من كلمة “تنوع” Diversity ) . وتوجد كل منظومة من الجينات على صبغي مستقبل . ويشبه انتظام جينات مستقبلة الخلية التائية إلى حد بعيد انتظام جينات السلسلة الثقيلة (Tonikawa ,S .1985 ) .
2.4- إعادة ترتيب الجينات Rearrangement
أوضحت الدراسات أن عددا كبيرا من الظواهر يحدث في المورثات المنتشرة على جزيئات ال ADN وتشكل RNA الرسول الآمر بتصنيع سلسلة الغلوبيلين المناعي . يمكن تمثيل إعادة ترتيب المجين في الضد ب (Fig.13) .
– أثناء تمايز Differentiation الخلايا الجينية إلى الخلايا اللمفاوية B فإن التعبير عن مورثات الغلوبيلينات المناعية لم يكن قد حدث بعد ، و في ذلك الوقت يحدث إعادة ترتيب المورثات على ال ADN . وهناك مورثات تكون في البداية متباعدة عن بعضها ثم تتقارب . و أخرى تلغى نتيجة لظواهر الحذف Deletion (شطب ، إلغاء قطع ال ADN ).
– أثناء تطور الخلايا اللمفاوية B، تصنع الأضداد النوعية حسب العمليات العادية لتصنيع البروتينات ثم تهاجر باتجاه الغشاء الخلوي مشكلة بذلك الأضداد الغشائية .
و تعتبر السلسلة الخفيفة في الضد الناتج تعبيرا لسلسلة من المورثات C,J,V. إن هذه المورثات الوظيفية منتقاة بصفة نهائية (من بين المورثات C,J,V الناتجة من إعادة ترتيب ADN) أثناء فقدان الإنترونات (القطع غير المشفرة ADN) التي ترافق هجرة ARNالرسول .و كل سلسلة لا تشرح إلا تغيرا واحدا لكل مورثة وعليه يمكن تقدير احتمالات التغير بأخذ الأرقام المعطاة (المقدمة) سابقا فنجد 150*5 تساوي 750 احتمالا متوقعا بالنسبة للمنطقة المتغيرة للسلاسل الخفيفة و 80*5*6=24000 احتمالا ممكنا بالنسبة للمنطقة المتغيرة للسلاسل الثقيلة و يكون بذلك مجموع الإتحادات الممكنة هو 750*24000=18000000 بالنسبة للضد الواحد .
و يمكن القول أن تركيب جين الضد اعتبارا من كسر مبعثرة يتم عبر مرحلتين ، تم تمثيلهما في الشكل السابق (13) فيما يتعلق بالسلسلة الخفيفة كابا .ففي المرحلة الأولى يتم وصل قطع من J و V تم انتقائها عشوائيا بواسطة إنزيمات تزيل كل ADNالذي يتوضع بين هذه القطع . و لقد تم في الشكل الترسيمي إزالة القطع J1 وV4 وV3 مما أدى إلى ضم الجينين J2و V2 أما في المرحلة الثانية فيتم انتساخ كامل ADN (من بداية V2 حتى نهاية الجين C ) إلى RNA . و تقوم الإنزيمات المعيارية لتضفير RNA ، والتي تسهم في تعبير عدد من الجينات بقطع كامل لل ARN الممتد من نهاية J2 وحتى بداية C. والمتوالية الناتجة التي تؤلف Messenger RNA ، تترجم إلى بروتين . (Tonikawa ,S. 1985 ) .
5- أهم وظائف الغلوبيلينات المناعية (Tab.2)
6- أهم مميزات صفوف الغلوبيلينات المناعية (Tab.3)
7- المستضدات Les antigènes:
يتعرف الجهاز المناعي على بعض المستضدات بصورة أفضل من غيرها، و عليه تصنف المستضدات إلى مستضدات قوية مثل البروتينات و عديدات السكر والليبيدات السكرية والفيروسات والجراثيم ومستضدات ضعيفة مثل الأحماض النووية والليبيدات الفوسفورية أما الدهون فتعتبر ناشبه Heptène لا تتمكن من توليد مناعة إذا لم ترتبط بحامل .
ومن جهة أخرى يوجد نمطان من المستضدات بالنسبة للإستجابة المناعية الخلطية أحدهما يتطلب تدخل الخلايا اللمفاوية T المساعدة لإنتاج الأضداد و يدعى بالمستضدات التابعة للغدة التيموسية في حين لا يتطلب النمط الآخر تدخل تلك الخلايا لإنتاج الأضداد و يدعى بالمستضدات غير التابعة للغدة التيموسية و ينتمي إلى النمط الأول البروتينات الحيوانية والجزيئات الكبيرة ذات البنية المعقدة والتي تحتوي على عدد كبير من المحددات Determents وينتمي إلى النمط الثاني عديد الوحدات
ذات الوزن الجزئي العالي و التي تملك عددا قليلا من المحددات Polymère.
B 8- المستقبلات الغشائية للخلية
تبنى كل خلية من ملايين الخلايا البائية على غشائها جزيئات بروتينية تكون ما يدعى بالمستقبل Récepteur membranaireالغشائي . تبقى هذه المستقبلات مرتبطة بالغشاء الخلوي و معروضة على السطح كجزيئات مستقبلة و هي عبارة على أضداد من صنفIgD و IgM .
عندما يغزو مستضد ما الدم فإن كل خلية بائية تجابهه بمستقبلاتها الغشائية حيث يتم التعرف على محدداته بالمستقبلات النوعية .وبذلك يتم الارتباط بين المستضد و الخلية البايئة وهو ما يحثها على الإنقسام والتمايز إلى نسيلة من الخلايا البلازمية . وتفرز هذه الخلايا أضدادا لها نفس خصائص الارتباط بالمستضد ، التي تتمتع بها الجزيئات المستقبلة الموجودة على سطح الخلية البايئة الأم .
ـ 9 الإستجابة المناعية الخلطية
تعرف الإستجابة المناعية الخلطية بأنها آلية الدفاع التي تستعملها العضوية لإنتاج الأضداد للقضاء على المستضدات . ويمكن للخلية البائية أن تتعرف على المستضد مباشرة بفضل مستقبلاتها الغشائية أو قد تستعين في التعرف عليه بالخلايا التائية المساعدة Th .
1.9 ـ مراحل الإستجابة المناعية الخلطية
أولا – مرحلة تحضير مولد الضد
و في هذه المرحلة تقوم البلاعم الكبيرة بالتعرف على المستضد و ذلك عن طريق محدداته فتبتلعه و تفككه إلى قطع صغيرة ثم تعرضه بشكل مهضوم جزئيا على سطحها و ذلك بفضل جزيئات المعقد النسيجي CMH2) 2 من الصنف (وبذلك يصبح المستضد جاهزا للتعرف عليه من طرف الخلايا التائية المساعدة .
ثانيا – مرحلة التعاون
تفرز الخلايا البالعة انترلوكين (IL-1) 1 الذي يؤثر على الخلايا اللمفية Tn التي تتعرف حينئذ على المستضد الذي قدم لها فتتنشط وتنقسم عدة انقسامات و بذلك يتشكل عدد كبير من الخلايا Th الناضجة . و هذه تستطيع أن تقوم بوظائفها حيث أن بعضها يبقى في الدوران الدموي أو اللمفي محتفظا بذاكرة الضد ، حيث تتصدى بسرعة أكبر للمستضد من نفس النوع يدخل الجسم فيما بعد . كما أن البعض الآخر من الخلايا التائية المساعدة الناضجة يقوم بإفراز انترلوكين2 (IL-2) وذلك لتنشيط الخلايا البائية النوعية لنفس المستضد .
ثالثا – تنشيط و تمايز اللمفاويات B
تنشط الخلايا البائية انترلوكين-2 فترتبط بالخلية Tn التي نشطتها ثم تنقسم عدة انقسامات تحت تأثير سيتوكينات أخرى تفرزها Tn منها مثلا :
BCGF (B Cell proliferiting Factor) BCFF ،(B Cell Granth Factor)
و ذلك لتنشيط و تكاثر الخلية B وزيادة النسيلات . ثم تفرز الخلايا Tn سيتوكينات أخرى تدعى بعوامل التمايزIL-4 مثلBCDF
وهو يعمل على تمايز خلايا بلازمية تقوم بإفرازالأضداد النوعي للمستضد ، ثم تفرز الخلايا وتقوم هذه الأضداد بوظائف عديدة للقضاء على الجسم الغريب (المستضد) لحماية الجسم من العدوى والأمراض فقد تقوم بتعديل كمية المستضد و قد تقوم بترسيبه وقد تنشط المتمم وقد تقوم بدور طاهيات .
و بالنسبة لمواقع تخليق الأضداد فقد بينت الدراسات أن السلسلة الثقيلة و الخفيفة تتكونان بشكل مستقل عن بعضهما حيث تتكون كل منهما على صنف مختلف من الريبوزومات الموجودة على الشبكة الأندوبلازمية ويستغرق تخليق السلسلة الخفيفة 30 ثانية بينما يستغرق تخليق السلسلة الثقيلة 60 ثانية ، و تنقل جزيئات البروتينات المناعية عبر جهاز كولجي و منها إلى صهاريج الشبكة الأندوبلازمية الملساء (الكبيسي،2001 )
: 2.9منحنى الإستجابة المناعية الخلطية
تمر الإستجابة المناعية الخلطية بثلاث مراحل أساسية هي على التوالي :
1-الطور التمهيدي
2-طور تزايد الأضداد
3-طور تناقص الأضداد
و يمكن تمثيل منحنيات الإستجابة المناعية الخلطية بالشكل التالي : (Fig .14)
1.2.9- الإستجابة الأولية
و هي الإستجابة المناعية التي تحدث نتيجة أول تماس مع المستضد .وتتميز بمايلي :
1.الطور التمهيدي :
يكون طويل حيث يستمر أسبوعين ، و يكون فيه معدل الأضداد قليل ، يتم خلال هذا الطور عملية التعرف على المستضد و تقديمه للخلايا Th ، و تنشيط الخلايا البائية حتى مرحلة تكوين الأضداد .
2.طور تزايد الأضداد :
تزداد الأضداد خلال خمسة أيام تقريبا لتصل إلى الحد الأعظمي و يكون معظمها من صنف IgM .
3.طور تناقص الأضداد :
يتميز بأن التناقص في الأضداد يكون سريعا .
2.2.9-الإستجابة الثانوية :
و هي الإستجابة التي تحدث عند تماس نفس المستضد للمرة الثانية وتمر بنفس الأطوار ، وتتميز بمايلي : (Fig.14)
. قصـر الطور التمهيدي.
.IgG.أغلب الأضداد تكـون من صف
.تناقص معدل الأضداد يكون بطيئا .
Complément – 10المتممة
1.10- تعريف المتممة
هي مجموعة غير متجانسة من بروتينات غلوبولينية ، ذات أوزان جزيئية مختلفة مشكلة جملة أنزيمية التي تكون في الحالة الطبيعية في حالة راحة إذ تكون مكوناتها في حالة غير نشطة . أما في حالة دخول المستضد فتنشط الجملة المتممة .
2.10- مكوناتها
تتكون من 20بروتينا مختلفا ، منها 13 للمشاركة في التنشيط و7 لمراقبة هذه الأخيرة .
نرمز لكل مكون من مكونات المتممة بالحرفC مرفق برقم وإذا تم تنشيط المكونات ، نرمز لهاCبحرف فوقه مطة و بعد التنشيط تنقسم مكونات المتممة إلى جزئين و يرمز لنواتج التفككbوaبالحرفين
،أما إذا فقد أحد مكونات المتممة نشاطه اصبح غير فعالinactive
(الكبيسي،2001 ) فيضاف إلى كتابته الحرف الصغيرinactive) i)
3.10- تنشيط المتممة :
تنشط المتممة بطريقتين مختلفتين هما الطريق الكلاسيكي(Doc .1) Voie classique
.(Doc.2) Voie alterne والطريق المتناوب
نشاط و خصائص المتممة-4.10
يمكن التعرف على نشاط و خصائص المتممة بالرجوع إلى الوثيقة (Doc.3)
الثأثيرات البيولوجية للمتممة-5.10
(Doc.4) يمكن الإطلاع على الثأثيرات البيولوجية للمتممة في
11السيتوكينات-Cytokines
هي مواد كيميائية تحررها الخلايا المناعية كوسائط كيميائية:عندما تحرر السيتوكينات من طرفالخلايا وحيدات النوى Monocytes
تدعى بالسيتوكينات الأحاديةMonokines
وعندما تحرر من طرف الخلايا اللمفية تدعى باللمفوكينات Lymphokines
. أما عندما تصل بين الكريات البيض فتدعى بالسيتوكينات الداخلية Interleukins مميزات السيتوكينات Doc.5
المراجع و المصطلحات :
12 -المصطلحاتTerminologie
إنجليزية عربية فرنسية
Activation تنشيط(تفعيل) Activation
Alternate pathway مسلك تناوبي(بديل) Voie altèrne
Anaphy latoxine مواد تأقية Anaphylatoxine
Anticorp الضد Anticorps
Antigene المستضد Antigène
Antiserum المصل المضاد Antiserum
Antitoxin الترياق Antitoxine
Carrier حامل Porteur
Classical pathway مسلك كلاسيكي Voie classique
Complement متممة Complément
Constante region المنطقة الثابتة Région constante
Crystalisable fragment المنطقة المتبلورة Fragment cristallisable
Cytokines سيتوكينات Cytokines
Cytolyse immune التحلل المناعي الخلوي Cytolyse immune
Differentiation تمايز Différentiation
Deletion شطب(خبن) Délétion
Determinant محدد Déterminant
Disulphide bridge جسور ثنائية الكبريت Ponts désulfure
Diversity تنوع Diversité
Domain المجالات(المقاطعات) Domaines
Flexibility مرونة Flexibilité
Fragment antigene
binding(Fab) منطقة ارتباط المستضد Fragment antigène
binding(Fab)
Genome المجين(الطاقم الوراثي) Génome
Hepten ناشب Haptène
Hinge region منطقة المفضلة Région charnière
Histocompatibility توافق النسيجي Histocompatibilité
Humoral immunity المناعة الخلطية Immunité humorale
Immunoglobuline الغلوبيلينات المناعية Immunoglobuline
Immunology علم المناعة Immunologie
Interleukins سيتوكينات داخلية Interleukines
Lymphocyte B الخلية اللمفاوية البائية Lymphocyte B
Mastocyte خلية صارية Mastocyte
Membrane receptor مستقبلات غشائية Récepteurs membranaires
Memory ذاكرة mémoire
Memory cell خلية ذاكرة Cellule à mémoire
Monocyte خلية وحيدة النواة Monocyte
Monokines سيتونات أحادية Monokine
Neutralisation تعديل السمية Neutralisation
Opsonine طاهية Opsonine
Opsonization طهي(طهو) Opsonization
Passive immunity المناعة السلبية(المنفعلة) Immunité passive
Pathway مسار(مسلك) Voie
Phagocyt خلية بالعة Phagocyte
Plasmocyte الخلايا البلازمية Plasmocytes
Polypeptide عديد البيبتيد Polypeptides
Protease الأنزيمات المحللة للبروتين Protease
Rearrangement إعادة ترتيب Réarrangement
Response إستجابة Réponse
Tetanus الكزاز Tétanos
Variable region المنطقة المتغيرة Région variable
:Bibliographie قائمة المراجع
1.أرحاب وآخرون(1993) :المناعة للثالثة ثانوي
دار الشريفة الجزائر ص 11-75
2.باسترنك.ت(1986) :الجهاز المناعي من كتاب مدخل إلى الكيمياء الحيوية
ترجمة أحمد كرزة منشورات جامعة حلب كلية الطب ص233-269
3.تولى.س.بوري(1977) :بسائط علم المناعيات
ترجمة محمد هيثم الخياط(1980) دار دلفين للنشر ميلانو إيطاليا ص2-34
4.تونيكاوا.س(1985) :جزيئات الجهاز المناعي
مجلة العلوم المجلد5 العدد3 سبتمبر 1988 ص94-105
5.خالد الكبيسي(2001) :علم المناعة و الأمصال
دار صفاء للنشر والتوزيع ط1 عمان الأردن ص 51-70
6.سويسي حسينة و آخرون(1990) :العلوم الطبيعية للسنة الثالثة ثانوي
المعهد التربوي الوطني الجزائر ص128-132
7.رفيق عبد الرحمان صالح(1990) :علم المناعة و الفحوصات المناعية
دار الفكر للنشر و التوزيع .مصر
8.ماراك ج و كايلر(1986) :الخلية التائية و مستقبلاتها
مجلة العلوم المجلد6 العدد8 اغسطس 1989 ص72-84
9.محمد ناجح الأغبر(1990) :المناعة و المرض
مطبعة الخالدية أبو ظبي ص11-27
10.يونك ،ج.د.إ و كوهن،ز.(1982) :الخلايا القاتلة كيف تقتل
مجلة العلوم المجلد6 العدد7 يوليو 1989 ص38-45
11.Benjamini ,A et Leskowitz ,S(1991) :Immunology
Ashort course second edition Wiley-Liss P1-148 .
12.Boden ,J.P et Al(1989) :Biologie terminale D
Bordas Paris P272-313.
13.Borden ,J.P et Al(1988) :Biologie premières A&B
Bordas Paris P
14.Bruce ,A et Al(1988) :Biologie moleculaire de la cellule
Flammarion medecine sciences P978
15.Collec ,Yves et Al(1989) :Biologie Géologie
Terminale D Nathan P242-243.
16.Rabhi Hocine(1993) :Immunologie générale
Office des publications universitaires Alger P125-157.
17.Tonegawa ,Susumu(1985) :Les molécules du système immunitaire
Pour la science n°98 P106-118 .
نظام المتمم-The Complement System 2
تحطيم المتمم خارج الجسم (في الزجاج) The Destruction of complement in vitro
يمكن تحطيم مكونات المتمم خارج الجسم بأحد الطرق التالية:
1- باستخدام المواد المانعة لتجلط: وهذه تعمل علي ازالة ايونات الكالسيوم من المكون C1 مما يؤدي الي تحللة وكذلك ازالة المغنيسيوم يؤدي الي منع تحول او تنشيط المكون C3 في المسلكين.
2- الحرارة: بتسخين المصل لمدة 30 دقيقة عند حرارة 56 درجة مئوية يؤدي الي تحطم مكونات المتمم.
3- التخزين: بالتخزين يتحول المصل الي مضاد للمتمم ويكون التأتير اكثر علي المكون C4.
4- المتبطات الطبيعية في المصل كالتي تعمل علي ازالة C1r وC1s من المكون C1 او المانعة لتنشيط المكون C1.
انتاج مكونات المتمم Complement synthesis
بروتينات المتمم يتم انتاجها بواسطة العديد من الخلايا، كما يمكن أن تنتج في المزارع الخلوية، بالاضافة الي القطع النسيجية، ولكن تعتبر الكبد المنتج الرئيسي لمعظم بروتينات المتمم، كما ان الخلايا البلعمية النسيجية، والارومات الليفية (fibroblast) هي الاخري قادرة علي تصنيع بعض من مكونات المتمم. اضافة إلي ذلك يؤدي الالتهاب إلي زيادة انتاج مكونات المتمم، ربما من خلال تأثير الانترلوكين-1 (IL-1) والجاما-انترفيرون (-interferon). خلايا الكبد بشكا اساسي تنتج كل من المكون C3 وC6 وC9 والعامل B، ويعتبر الكبد العضو الرئيسي لأنتاج كل من المكون C3 والعامل B. الخلايا الطلائية للأمعاء تنتج المكون C1، وتنتج خلايا وحيدات النواة المكون C2، بينما يتم أنتاج العوامل C4 وC2 وC3 وC5، وفحين ان العامل B بواسطة الخلايا البلعمية الكبيرة (macrophage).
عواقب الانشطة البايولوجية للمتمم (The Biological Consequence of complement Activation) :
تنشيط المتمم بالطريق التقليدي او البديل اضافة الي الدور الدفاعي الذي تقوم به من خلال تخريب الغشاء الخلوي وتحلل الخلية فايضا تفعيل المتمم يؤدي الي تكوين العيديد من الببتيدات المهمة التي تدخل في فعاليات الالتهاب، حيت أن اطلاق وارتباط اي منهما مع الخلايا الصارية او البازوفيل يؤدي بهما الي افراز الهستامين الذي يسبب زيادة في نفادية الاوعية الدموية الشعيرية، مما يشجع الكريات البيضاء (الخلايا الاكولة) علي الهجرة الي منطقة الاصابة (الالتهاب) او منطقة شدة الحساسية . كما أن الـ C3a والمعقد المتكون من C5b67 تعتبر عوامل جادبة لبعض الكريات البيضاء اي أن هذه المعقدات تشجع الكريات البيضاء علي الهجرة الي الاماكن النسيجية التي تجرى فيها الفاعليات المناعية . ايضا المتمم له خاصية الالتصاق المناعي والتي تتم بواسطة قطعة المتمم الثالثة (C3a)، والخلايا التي تحمل مستقبل خاص لجزئ المتمم C3a تميل الي الالتصاق بكريات الدم البيضاء وكذلك بخلايا اخري مما يشجع علي عملية البلعمة والالتهام .
في بعض الاحيان يؤدي تنشيط المتمم الي احداث اضرار نسيجية خاصة ببعض الامراض وهناك سببين في الغالب لحدوث لذلك هي :
1- التنشيط بواسطة الاجسام المضادة الذاتية . 2- التنشيط بواسطة المعقدات المناعية المتكونة .
الثأتيرات البايولوجية لتنشيط مكونات المتمم
C3a:تعمل كمسبب لتأقئ من خلال تقليص العضلات الملساء، زيادة نفادية الاوعية الدموية، كما تسبب خسف حبيبات الخلايا الصارية في الجلد والبازوفيل مؤدياً الي افرازها للهستامين، كما تعمل علي الصفائح الدموية مؤديا بها الي افراز الهستامين والسيرتونين (Serotonin).
C3b:تشجيع عملية البلعمة (بواسطة الالتصاق المناعي) واذابة المعقدات المناعية لتسهيل بلعمتها والمشاركة في التنظيم المناعي.
C4a:تقلص العضلات الملساء وزيادة نفادية الاوعية الدموية.
C2a:يؤدي الي زيادة نفادية الاوعية الدموية الشعيرية.
C5a:تعمل كمسبب لتأقئ من خلال تقليص العضلات الملساء وزيادة نفادية الاوعية الدموية، كما تسبب خسف حبيبات الخلايا الصارية في الجلد والبازوفيل مؤدياً الي افرازها للهستامين، كما يسبب تنشيط وجدب النتروفيل ويؤدي بها الي افراز الانزيمات الهاظمة (lysosomal).
C5b67:يساهم في الجدب الكيميائي للكريات البيضاء.
تتمكن الاجسام المضادة الذاتية وكنتيجة ثانوية لحدوث تخريب نسيجي او الاصابة او نتيجة لعوامل اخري غير معروفة أن ترتبط بمستضدات هذه الانسجة الذاتية المعطوبة مما يؤدي الي تنشيط فعالية المتمم ضد النسيج الداتي، كما في حالة فقر الدم التحللي المناعي الداتي (auto-immunohemolytic anaemia) الذي يحدت بسبب انحلال كريات الدم بواسطة تنشيط المتمم.
أن عملية تنشيط المتمم في الخلايا الخاصة بجدران الاوعية الدموية الصغيرة بواسطة المعقدات المناعية المتكونة موضعيا، او التي تترسب من الدم تؤدي الي حدوت تلف نسيجي والتهاب ينتج عنة تهدم هذه الاوعية الدموية، وتعرف هذه الحالة بأسم Arthus، كذلك هذه العملية هي المسؤولة عن مرض المصل المناعي (serum sickness)، وربما بعض الامراض السرطانية وامراض المناعة الذاتية. وفي حالة الالتهاب الرثواني (Rheumatoid arthritis) بسبب تراكم المعقد المناعي في اغشية المفاصل فأن ذلك يؤدي الي حدوث التهاب المفاصل المتعدد بسبب تنشيط المتمم.
الاشخاص المصابين بمرض الدؤب الاحمراري الجهازي (Systemic Lupus Erythematosis) والافات الجلدية والتهاب كبيبات الكلية كلها حالات سريرية لترسب المعقدات المناعية تؤدي الي تنشيط المتمم.
– يحتوي سم افعي الكوبر مادة بروتينية تسمي العامل السمي للكوبرا (cobra venum factor) تعمل علي تنشيط المسلك البديل بمكانيكية فريدة، ويعتبرهذا العامل نظير للـC3 convertase. وهذا الانزيم مقاوم لتثبيط بالعوامل H وI وبالتالي فأن الانزيم ينشط المتمم باستمرار وبذلك يستهلك المتم.
تنظيم تنشيط المتمم Regulation of complement activation
أن عواقب تنشيط المتمم قد تكون ذات أهمية بالغة في دفاعات العائل أو قد تكون ذات عواقب خطير علي صحة العائل، ولهذا يتطلب أن يتم السيطرة علي تنشيطها بشكل محكم وذلك حسب الحاج الي تنشيطها من عدمة وتتم السيطرة علي تنشيط المتمم بواسطة البروتينات المسيطرة والمنظمة لعمل المتمم والتي اغلبها يعتبر جزء من مكونات بروتينات المتمم والتي كما اشيرة اعلاة يبلغ عددها اكثر من 30 بروتين.
مثبط المكون C1 (C1 inhibitor) يعتبر اهم منظم في تنشيط المسلك التقليدي لتفعيل المتمم، وهذا المتبط يعمل علي التحكم في تكوين المعقد C4b2b من خلال الارتباط مع وغلق او وقف تنشيط الوحدة الفرعية C1r وC1s، كما توجد عدة بروتينات سكرية اخري تتولي تنظيم تنشيط المكون وفي المسلكين التقليدي والبديل بالنسبة للمكون C3b وC4b
العوز في مكونات المتمم Complement Deficiency
يمكن تقسيم حالات النقص في مكونات المتمم الي قسمين خلقي ومكتسب.
النقص الخلقي:
لقد تم الكشف عن عوز مكونات المتمم بسبب العوامل الوراثية في العديد من الحالات المرضية، وقد وجد بأن هذا العوز قد يحدت في اي من مكونات المتمم بما فيها المثبطات (مثل متبط الـC1) والمنظمات. وعادتا يكون هذا النقص ناتج عن عدم انتاج المكون او قلة في انتاجه او أن يتم أنتاج المتمم مع وجود خلل في تركيبه مما يجعلة غير فاعل (خامل) او يتم انتاج المتمم ولكن يتم تهدمة بسرعة او يتم مع انتاجة، انتاج مواد مضادة للمتمم. وتكون نتيجة العوز في احد او بعض مكونات المتمم في هذه الحالة جعل العائل اكثر عرضة للأصابات المرضية.وتكون الحالة اكثر خطورة عندما يكون النقص في المكون الثالث (C3).
النقص المكتسب:
النقص المكتسب عادتا يكون مصاحباً للمعقدات المناعية الدائرة في الدم، كما هو الحال في مرض الدؤوب الاحمراري، وهذا المرض يتميز بقلة المتمم C1 وC4 وC2 وC3 في المرحلة الاولي للمرض وتعود الي تركيزها الطبيعي في حالة الشفاء من المرض.
المرضي المصابين بنقص مكونات المتمم التي تعمل في المرحلة الاولي للمسلك التقليدي عادتاً ما يظهرون علامات مرضية مصاحبة لأمراض الانسجة الرابطة، اما المرضي المصابين بقلة المكونات الاخيرة للمتمم مثل المكون C5 او C6 او C7 او C8 فيكونوا حساسين للأصابة بجرثومة الـNeisseria، بينما المصابين بنقص في المكون C3 والمكون C5 فيصابون بأصابات قيحية، وايضا المصابين بنقص العوامل المنشطة للمسلك البديل يتعرضون للاصابات القيحية . النقص المكتسب يكون في الغالب مؤقت حيث أنه ما أن يزول السبب حتي يعود المكون او المكونات الناقصة الي مستوياتها الطبيعية.
اللقاحات Vaccines
اللقاح أو الطعم:
هو عبارة عن مستضد قادر علي أحداث المناعة وغير قادر علي أحداث المرض.
التلقيح أو التطعيم Vaccination
وهي عملية تعريض أو إعطاء شخص ما بشكل عمدي الجراثيم (اللقاح أو الطعم) المسببة للمرض حية أو ميتة أو سمومها المختزنة لغرض حث الجسم علي تكوين حالة من المناعة ضد تلك الجراثيم أو ضد سمومها دون أن يكون لتلك الجراثيم أو سمومها القدرة علي أحداث المرض.
أنواع اللقاحات:-
تصنف اللقاحات حسب نوع المادة التي أعدت منها و طريقة أعدادها كما يلي:-
1- اللقاحات الحية المضعفة ( Live attenuated vaccines) :- وهي عبارة عن لقاحات تحتوي علي معلق لجراثيم أو فيروسات حية تم أضعافها بالحرارة أو الزراعة المتكررة بحيث تفقد قدرتها علي أحداث المرض واحتفظت بقدرتها علي استثارة تكوين مناعة فاعلة.
أهم اللقاحات الحية المضعفة:-
ا- لقاحات فيروسية مضعفة مثل:- لقاح ضد النكاف ((Mump) ، لقح الجدري Smallpox)) ، لقاح الحصبة (Rebella) و لقاح الحصبة الألمانية (Measles)
ب- لقاحات جرثومية مضاعفة مثل : لقاح التدرن (السل) (BCG)
2- اللقاحات الميتة (Killed Vaccines) :- وهي عبارة عن لقاحات تحتوي علي معلق من الجراثيم أو الفيروسات المقتولة بالحرارة أو المعالجة الكيميائية أو الإشعاعية ومن أمثلتها:-
ا- لقاحات جرثومية ميتة :- مثل لقاح التيفود (Typhoid) ، لقاح السعال الديكى (Pertussis or whooping cough)
ب- لقاحات فيروسية ميتة مثل :- لقاح السعار (داء الكلب) (Rabies) ولقاح الأنفلونزا (Influenza)
3- السموم المختزلة ( Toxoid): وهي السموم الخارجية التي تفرزها بعض الجراثيم وضعفت بالحرارة أو المعالجة الكيميائية (الفورمالين) بحيث تفقد سميتها وتحتفظ بقدرتها علي تكوين المناعة مثال ذلك لقاح الخناق (Diphtheria) ولقاح الكزاز.(Tetanus) وهذا النوع من اللقاحات عادتا يعطي مرتين ليكون مناعة فعالة جرعة مقوية أولى تم تعقبها جرعة ثانية قد تعقبها جرعة مقوية (معززة Booster).
4- لقاحات مشتقات الجراثيم Bacterial Deviate Vaccines:-وهي لقاحات تستخدم فيها أجزاء معينة من الجراثيم تحتوي علي مستضدات تلك الجراثيم مثل شعيرات الجراثيم (Pili) المسببة لمرض السيلان (الزهري) (Syphilis) ومن أمثلتها لقاح السيلان ولقاح التهاب السحايا (Polio).
5- لقاحات ضد الحيوانات الأولية والدودية Protozoa and Helminthic Vaccine:- الحيوانات الأولية والدودية طفيليات معقدة تنتج الكثير من المستضدات علي سطحها وكذلك من خلال نتائج العمليات الايضية فيها. كما تظهر مستضدات مختلفة خلال مراحل التطور التي تمر بها لذا فأنه من الصعب عمل لقاح ضدها . أن التحصين بواسطة بيض الديدان الشريطية المضعفة قد أعطى نتائج مقبولة إلى حد ما . كما أن الأبحاث قائمة لأجاد لقاح مضاد للملاريا وغيرها من الطفيليات.
